姜格宁,张雷,朱余明,陈昶,周晓,刘锦铭,张鹏,汪浩,谢博雄,王海峰,蒋雷,范江,赵德平,陈乾坤,段亮,何文新,周逸鸣,刘鸿程,赵晓刚,秦雄,杨洋
上海市肺科医院 胸外科(上海 200433)
【关键词】 肺切除;肺功能;评估;共识
外科手术是治疗肺部疾病的重要手段,但临床工作中时常遇到合并受损肺功能状态的患者。肺通气或弥散功能的下降,增加患者围术期并发症风险,并影响远期生存率。术前需要根据患者的疾病分期,拟定切除范围,结合患者肺功能状况,评估并预测患者围术期并发症风险以及远期生活质量,综合利弊,以决定是否行外科手术,以及手术切除的范围。
1679 年,Borelli 等首次检测患者呼出气体的容积,被视为是人类肺功能检测的开端。肺功能的检测在胸外科已应用 50 多年,1971 年,Boush 等发现第一秒用力呼气容积(FEV1)可作为胸外科术前评估手术耐受的重要指标。此后,在一项对 2340例患者的研究中,Miller 等使用 FEV1 结合最大通气量(MVV)及用力呼出气量为 25%~75% 肺活量时的平均流量(FEF25%~75%), 建立更为准确的肺切除手术患者的筛选标准和方法,有效降低了肺切除患者术后的死亡率。1987 年,Bechard 等提出,心肺运动功能试验由于其同时检测了心、肺的负荷功能,有效模拟了肺切除术后患者的状态,可作为肺切除术前评估的重要检测方法,同时证实了运动中最大摄氧量(VO2max)<10 mL/(kg·min),与术后并发症和死亡率显著相关。1988 年,Ferguson 等证实了肺一氧化碳弥散量(DLCO)在肺癌术后患者预后判断中的作用,自此 FEV1 和 DLCO 开始被作为肺癌术前评估的标准指标。1999 年,Wyser 等使用 FEV1、DLCO、VO2max、预测术后第一秒用力呼气容积(PPO-FEV1)以及预测术后肺一氧化碳弥散量(PPO-DLCO)作为肺癌术前筛选标准,该方法使肺切除术后,患者并发症发生率进一步下降50%。此后英国胸科协会(BTS)、欧洲呼吸学会/欧洲胸外科医师学会(ERS/ESTS)、美国胸内科医师学会(ACCP)等组织相继发布相关指南,指导术前肺功能评估。
术前肺功能评估的目的:使用无创或者微创的方法,准确评估患者肺功能,预测患者接受根治性手术后,围术期并发症的风险及远期生存风险,为外科手术切除范围决策提供依据。根据评估结果,采取有效防治措施,从而降低相关并发症发生率,提高远期生活质量。
1 方法与证据
本共识检索了 PubMed 和 Web of science 数据库近 20 年的相关文献和研究资料,结合国际现行临床指南,旨在给予临床一线医生规范化术前肺功能评估以指引和参考。
本共识撰写修订历经 18 个月,期间召开专业委员会会议 6 次,各专家间私下交流不做记录。2018 年 5 月 8 日,各专家讨论本共识涉及范围及检索资料相关内容分析;9 月 4 日,各专家分配各自负责领域相关内容的撰写和分析。2019 年 3 月 5日,委员会将所有内容汇总,进行第一次集体讨论,制定排版顺序;5 月 14 日,所有专家到会,对每个部分的内容进行审校,互相提出修改意见;8月 6 日,对所有上一次会议提出的修改意见,逐条分析修改;9 月 24 日,委员会将共识全文通读提出最后修改意见,定稿完成。
本共识的推荐级别为:ⅠA 级:风险与收益明确,基于无缺陷随机对照临床试验结果,强烈推荐,无保留地在各种环境应用于绝大多数患者;ⅠB 级:风险与收益明确,基于有缺陷的随机对照临床试验结果,强烈推荐,可应用于绝大多数患者;ⅠC 级:风险与收益明确,基于观察性研究结果,中度推荐,可能因可靠的研究证据出现而改变。
2 肺通气与弥散功能
2.1 肺通气功能的测定
FEV1 及 PPO-FEV1 是用于评估风险的主要通气功能指标。FEV1 和 PPO-FEV1 的下降,提示存在术后并发症和围术期死亡风险增加。经典的指南主要通过 FEV1 绝对值,作为初步筛选的指标:FEV1>2.0 L 可行全肺切除术,>1.5 L 可行肺叶切除术,此类患者不需要进一步的评估。
患者个体差异较大,不同体格患者的 FEV1 差异显著,仅凭借 FEV1 绝对值筛选患者可能存在偏差。根据患者性别、身高、体重、年龄等因素,从大宗数据统计建立模型,推算患者预计肺功能,采用FEV1 占预计值比例,较好地解决了个体差异问题。多数研究显示:PPO-FEV1<40% 预计值,提示围术期并发症发生率升高,据文献报道发生率为 16%~50%。Nakahara 等的研究提示:如PPO- FEV1 <30% 预计值,患者围术期死亡率为60%。因此,经典文献将 PPO-FEV1<40% 预计值,作为评估手术高风险的阈值。
PPO- FEV1 计算公式:对于全肺切除患者:PPO-FEV1=术前检测 FEV1×(1-所切除侧肺功能所占功能比例)
对于肺叶切除患者:PPO- FEV1 =术前检测FEV1×(1-具有功能并将被切除的肺段数量/具有功能的肺段数量)随着研究的进一步开展,通气功能的筛选阈值也在发生着一定的变化。同时研究提示 FEV1 是可用于预测手术风险的独立危险因素,患者术前FEV1<30% 预计值,围术期呼吸系统并发症发生率为 43%,而在 FEV1>60% 预计值的患者中发生率仅为 12%。Ferguson 等的一项包括 1 046 例患者的研究中提示,FEV1 是预测围术期因肺部并发症死亡的独立危险因素(OR=1.1/FEV1 下降 10%),也同样是围术期因心血管并发症死亡的危险因素(OR=1.13/FEV1 下降 10%)。Licker 等对 1 239 例患者进行了研究,提示 FEV1 是可以用于预测手术并发症的指标,同时确认了 60% 预计值为最佳的筛选阈值。
2.2 肺弥散功能的测定
弥散功能主要是通过 DLCO 来实现的。1988年,Ferguson 等发现 DLCO 是预测肺切除术后并发症和死亡的独立因素,DLCO<60% 预计值的患者,术后呼吸系统并发症发生率为 40%,围术期死亡率为 25%。Berry 等对 340 例患者进行了研究,提示 FEV1 和 DLCO<60% 预计值的肺叶切除患者,围术期死亡率为 5%,并发症发生率为 48%,FEV1和 DLCO 均为独立的危险因素。Cerfolio 等对906 例患者进行研究,证实 DLCO 与 FEV1 同样为重要的预测指标。同时他们提出 DLCO 与肺疱容量比值占预计值百分比(DLCO/VA%)是另一个重要的预测肺切除术后并发症的指标。随着相关研究的开展,学者们发现 DLCO 与肺切除术后患者的长期生存存在相关性。Liptay 等的研究提示,消除 FEV1 的影响后,患者以不同的 DLCO 进行分组,远期生存率随 D L C O 的下降而不断降低。
Ferguson 等在单因素分析中发现,DLCO<60% 预计值组相比于>80% 预计值组,危险比(HR)为1.35,运用多因素分析发现 DLCO 是患者长期生存的独立预测因素。
对于拟行肺部手术患者,目前国际指南均推荐同时使用 FEV1 和 DLCO 进行评估,并同时计算PPO-FEV1 和 PPO-DLCO。ERS/ESTS 指南的初筛标准仍采用术前 FEV1 和 DLCO,如均>80% 预计值,则无需进一步评估,可行预期手术;而 ACCP 指南则在初筛时,就要求根据切除范围进行 PPO-FEV1和 PPO-DLCO 的计算和评估,如均>60% 预计值,则无需进一步评估,可行包括全肺在内的手术治疗。
PPO-DLCO 计算公式:对于全肺切除患者:PPO-DLCO=术前检测DLCO×(1-所切除侧肺功能所占功能比例)对于肺叶切除患者:PPO-DLCO=术前检测DLCO×(1-具有功能并将被切除的肺段数量/具有功能的肺段数量)
PPO-FEV1 和 PPO-DLCO 的计算需要明确有效肺段数量以及需要切除的有效肺段数量。无论是肺叶、肺段、联合肺段(亚段)、联合肺叶切除手术,都可根据指南提供的计算方式,通过对 PPOFEV1和 PPO-DLCO 的计算来评估患者肺功能情况。如实际情况比较复杂,如切除肺组织部分或非手术切除部分肺组织存在功能不一致(有无效区域或者非均质病变,尤其是对于伴有非均质分布的肺部弥漫性疾病的患者),需借助 CT 或核素肺灌注-通气扫描检查,评估有效肺单位的数量,从而更精准地预测 PPO-FEV1 和 PPO-DLCO。相关研究显示,术前 CT 三维重建可用于 PPO-FEV1 和 PPODLCO的评估。Le Roux 等采用镓-68 与锝-99 结合大颗粒聚合白蛋白肺灌注,正电子发射计算机断层显像(PET/CT)检测 22 例拟行肺手术患者,术前及术后肺功能的检查和随访发现不同肺叶的肺功能在不同患者中存在明显个体差异。
推荐意见:(1)对于拟行根治性手术的患者推荐检测患者的 FEV1 和 DLCO,并且根据患者手术切除范围,对患者的 PPO-FEV1 和 PPO-DLCO进行计算和评估(推荐级别:ⅠB 级)。
(2)对于拟行根治性手术的患者,根据拟切除范围,患者的 PPO-FEV1 和 PPO-DLCO 均>60%预计值,则无需进一步评估,可按原计划进行手术切除治疗(推荐级别:ⅠC 级)。
(3)对于拟行根治性手术的患者,根据拟切除范围,患者的 PPO-FEV1 或 PPO-DLCO<60% 预计值,且二者均>30% 预计值,则推荐采用低科技运动功能试验,包括:登楼试验、往返步行试验等(推荐级别:ⅠC 级)。
(4)对于拟行根治性手术的患者,根据患者手术切除范围, 患者的 P P O - F E V 1 或 P P O -DLCO<30% 预计值,则推荐进行心肺运动功能试验对患者进行评估,检测患者 VO2max(推荐级别:ⅠB 级)。
3 低科技运动功能试验
3.1 登楼试验
登楼试验是一种简易的心肺功能运动试验,不需要特殊的设备或过多的人力。登楼时,患者需要动员大量肌肉参与此运动,与其他运动相比,对患者具有一定压力,在一定程度上反映了患者心肺功能情况。1987 年,Bolton 等证实了登楼试验和肺功能之间的对应关系:可以登上 3 楼提示 FEV1>1.7 L,5 楼则提示 FEV1 >2.0 L。登楼试验的局限性:因患者爬楼的速度、楼层的高度、患者的体重等因素,均可能使结果发生巨大差异。针对这种情况,学者们进行了登楼试验的规范化研究。
(1)将楼层的层数改为登楼的总高度,Brunelli等对 160 例患者进行研究,发现登楼高度>14 m的患者术后心肺并发症发生率为 6.5%,而高度<12 m的患者心肺并发症发生率为 50%。2008 年他们的研究扩大了样本量,研究显示,与登楼高度>22 m的患者相比,<12 m 的患者心肺并发症发生率是前者的 2 倍,死亡率是前者的 13 倍。同时相关研究提示,登楼高度和心肺运动功能试验结果有着明确的相关性。爬楼高度<14 m 的患者中有 56% 患者VO2max<15 mL/(kg·min),而登楼高度>22 m 的患者中 98% 具有>15 mL/(kg·min)的 VO2max。
(2)患者的体重和登楼的速度,Novoa 等在最近的研究中,对患者的体重和登楼的速度建立了修正的公式,对低科技运动试验进行了一次有意义的探索。
综上,登楼试验可以在一定程度上了解患者心肺功能情况,但相对比较粗略,对于临界肺功能患者,采用心肺功能试验是更为稳妥的评估策略。
3.2 往返步行试验
往返步行试验是另一个简易心肺功能试验,要求患者在两个相距 10 m 的标记之间做往返运动,步行的速度由声音信号控制,速度随每分钟逐渐增加,直到受试者因气促,无法继续达到信号要求的速度为终止。在 Singh 等进行的一项研究中,2次均无法完成 25 个单程的受试者,提示其 VO2max<10 mL/(kg·min)。Win 等[30]的研究提示往返步行的距离和 VO2max 具有一定的相关性,但是往返步行试验可能低估患者的 VO2max。Benzo 等的研究则显示,往返步行试验和 VO2max 直线存在明确的关系,55 例完成 25 个单程的受试者,其 VO2max 平均值为 15 mL/(kg·min)。目前往返步行试验在临床使用较少,其对患者的临床肺功能评估效果略差于登楼试验,但仍可作为临床肺功能的一项补充试验,提高低科技运动试验评估的准确性。
3.3 6 分钟步行试验
因目前未存在详细定义的 6 分钟步行试验的方法和标准,且对 6 分钟步行试验的相关研究也较少,并且各研究之间存在明显不一致结果,目前国际上发布的指南不推荐使用该试验作为术前肺功能评估的方法。近期有研究对 6 分钟步行试验进行改良的方法,认为在 6 分钟步行试验时检测患者心率及氧饱和的变化,从而提高术前肺功能评估准确率,该类研究为低科技运动试验的改良提供了崭新的思路。
推荐意见:对于所有可能接受根治性手术的患者,如患者经往返步行试验后,步行≥25 程(≥400 m);或者经登楼试验,爬楼高度>22 m患者,术前评估为低风险患者。如患者经往返步行试验,步行<25 程(<400 m);或者经登楼试验,爬楼高度<22 m,则推荐进行心肺运动功能试验,对患者进行评估,检测患者 VO2max(推荐级别:ⅠC 级)。
4 心肺运动功能试验
心肺功能试验是一种比较复杂的生理学检测技术,需要对患者运动时的心电图、运动负荷心率、每分钟通气量和每分钟氧摄取进行实时记录。
该检测技术可以获得 VO2max,VO2max 是既往的指南所推荐作为评估患者心肺功能和手术耐受的重要指标,心肺功能试验是更为精确的手术风险评估模式。根据 ERS/ESTS 2009 年发布的指南,心肺运动功能试验推荐级别较高,对所有术前肺功能检测提示 FEV1 或者 DLCO 其中任一<80% 预计值的患者,均推荐进行心肺运动功能的检测来评估患者手术的风险。如患者心肺运动功能检测提示运动过程中 VO2max>20 mL/(kg·min)或者>75% 预计值,则患者可以行包括全肺在内的所有计划内手术;对于运动中 VO2max<20 mL/(kg·min)的患者则需要根据手术切除的范围进行 PPO- FEV1 和PPO-DLCO 的计算,如两者均>30% 预计值,则可以行计划切除范围的手术,如果其中有任何一项<30% 则需要根据手术的切除的范围对 PPO-VO2max进行计算,PPO-VO2max>10 mL/(kg·min)或者>35% 预计值则可行计划切除范围手术。
PPO-VO2max 计算公式:对于全肺切除患者:PPO-VO2max=术前检测 VO2max×(1-所切除侧肺功能所占功能比例)对于肺叶切除患者:PPO-VO2max=术前检测VO2max×(1-具有功能并将被切除的肺段数量/具有功能的肺段数量)
研究证实,患者术后的死亡风险与运动中的 VO2max 息息相关,VO2max<10 mL/(kg·min)的患者具有极高的术后死亡率。Benzo 等的一项Meta 分析显示(包括 14 项研究,955 例患者)术后发生并发症的患者比术后无并发症的患者,其VO2max 降低 3 mL/(kg·min)。Loewen 等对 346例患者研究发现,VO2max<65% 预计值提示术后更可能发生并发症,并且如果 VO2max<15 mL/(kg·min),则提示较差的远期生存,这些结果与之前的一些研究相一致,因此推荐更激进地使用心肺运动功能试验作为肺切除患者术前评估的方法。Bayram 等的研究提示,在 VO2max>15 mL/(kg·min)的患者中未发现术后心肺并发症的发生,而 VO2max<15 mL/(kg·min)不仅提示肺部并发症发生率明显增高,同时还提示了发生心血管并发症风险明显增加。
Torchio 等对 145 例接受肺切除手术的慢性阻塞性肺疾病(COPD)患者进行研究显示,心肺运动功能检测是评估此类患者术后心肺并发症的一个非常重要方法,并且认为使用 VO2max 及 V’E/V’CO2 的斜率是有效的评估指标。Bobbio 等的研究也给出了类似的结果,认为心肺运动功能试验中测得的VO2max 与患者的预后有明显相关性。Brunelli 等对 200 例患者进行研究显示,对于 VO2max>20 mL/(kg·min)的患者术后死亡率为 0%,心肺并发症的发生率仅为 7%,而对于 VO2max<20 mL/(kg·min)的患者术后并发症发生率提高 5 倍,而围术期死亡率提高 13 倍。
因患者的肺部疾病和长期吸烟,患者可能合并冠状动脉粥样硬化和心功能不全等状态,心肺运动功能试验同时可以对患者心肌血流灌注进行评价和检测,多个指南推荐心肺运动功能试验作为具有心肌缺血病史患者的术前评估方法,用于评估和了解患者心肌灌注储备和心功能情况。同时因心肺运动功能试验对患者是一种负荷试验,在进行检测前应对患者进行心功能的评估,避免患者在试验过程中诱发心血管事件。美国心脏学会/美国心脏病学会(AHA/ACC)[41]和欧洲心脏病学会/欧洲麻醉学会( E S C / E S A )推荐使用修正心脏风险指数(revised cardiac risk index,RCRI)来评估心脏疾病患者的手术风险。Brunelli 等对 1 696 例肺切除手术患者进行研究,结果显示四项指标与肺切除术后并发症息息相关,分别为:脑血管疾病(1.5 分);心肌缺血(1.5 分);肾功能异常(肌酐>2 mg/dL 或>176.8 μmol/L 1 分);全肺切除术(1.5 分),目前将此四项作为胸科心脏风险指数(thoracic RCRI,ThRCRI)。术前根据患者病史及相关检测对其进行评分,如 ThRCRI<2 分则无需进行进一步心脏功能评估,可直接进行肺功能评估,根据肺功能情况进行心肺运动功能试验。如 ThRCRI≥2 分,评估患者心肌灌注和心功能情况,如需要手术干预,则不进行包括心肺运动功能试验在内的其他评估,予以经皮冠状动脉介入治疗(PCI)或冠状动脉旁路移植术(CABG),治疗后 6 周,再次进行评估,进一步治疗。如患者虽然 ThRCRI≥2 分,但尚无手术干预指征,则患者在药物治疗和医疗干预下进行心肺运动功能试验和肺功能的相关评估。
综上所述,心肺运动功能试验,可在肺切除术前患者的风险评估中,发挥重要的作用。心肺运动功能试验的本质是运动负荷试验,可以同时评估患者心肺功能,不仅仅对肺部并发症,对心血管并发症也具有同样的评估作用,因其有效模拟了患者术后心肺工作的状态,可以更为准确和直观地进行评估。但心肺运动功能试验需要复杂的设备和专业的检测人员,目前在国内的开展情况比较局限,仅限于较大的临床中心,故其应用价值还未得到体现。
推荐意见:(1)对于拟行根治性手术的患者,如心肺运动功能试验提示 VO2max>20 mL/(kg·min)或者>75% 预计值,则患者归为手术低风险组,可以进行包括全肺切除在内的手术治疗(推荐级别:ⅠC 级)。
(2)对于拟行根治性手术的患者,如心肺运动功能试验提示 VO2max<10 mL/(kg·min)或者<35% 预计值,则患者归为手术高风险组,需要谨慎选择治疗方式,包括缩小手术范围重新计算并评估,或者选用非手术治疗方案(推荐级别:ⅠC级)。
(3)对于拟行根治性手术的患者,如心肺运动功能试验提示 VO2max 为 10~20 mL/(kg·min)或者 35%~75% 预计值,则需要根据患者切除范围计算 PPO-VO2max,如经计算后 PPO-VO2max>10 mL/(kg·min)或者>35% 预计值,则建议行所计算切除范围的手术治疗,但仍需注意患者手术风险为相对高风险(推荐级别:ⅠC 级,图1)。
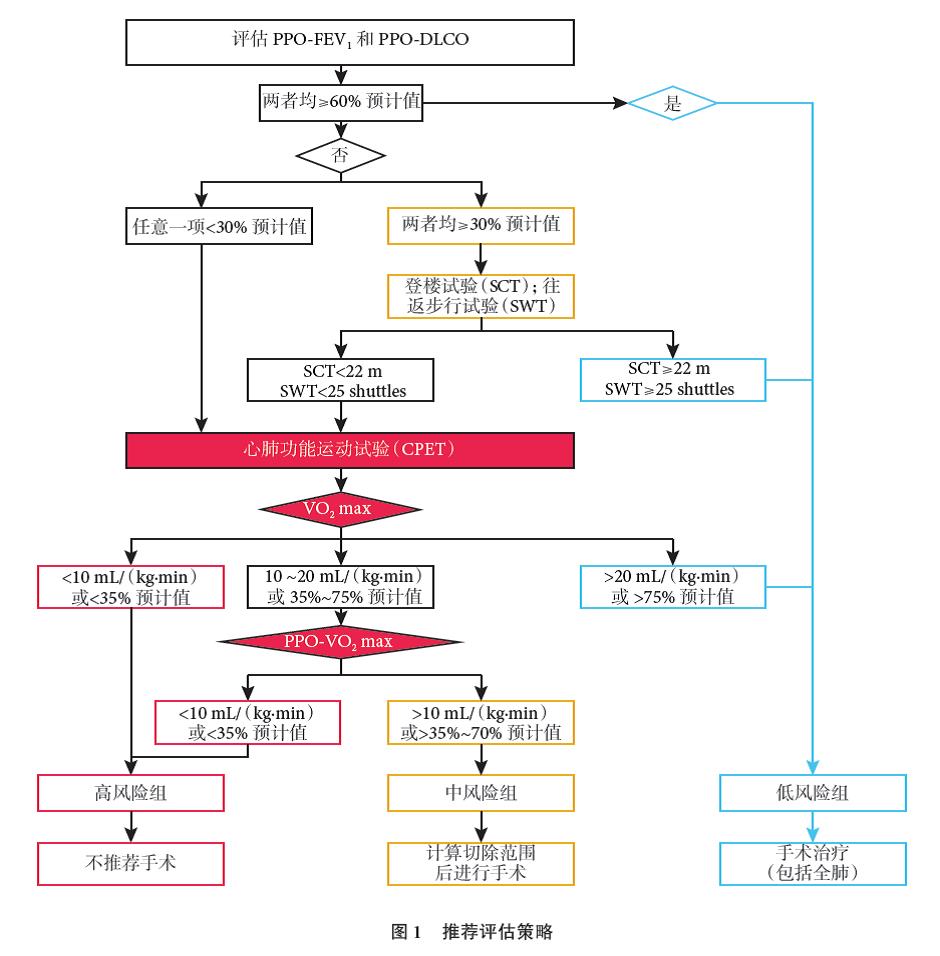
5 动脉血气分析
血气分析既往被视为肺部手术术前重要的评估指标,尤其在没有条件进行肺弥散功能检测时,动脉血气分析结合患者肺通气功能可在一定程度上评价患者肺弥散功能。既往认为高碳酸血症 [动脉血二氧化碳分压(PaCO2)>45 mm Hg] 被认为是相对的手术禁忌证,提示患者术后不良事件发生的可能性增大。相关研究显示,高碳酸血症不是肺切除手术围术期的独立危险因素。Stein 等的研究显示,PaCO2 >45 mm Hg 与术后患者死亡率无相关性。另外两个研究也显示了动脉血气分析提示高碳酸血症患者,围术期并发症发生率与正常患者相比无明显升高。而有研究显示,术前低氧血症患者围术期并发症发生率明显提高。同时血气分析可以在一定程度上反映患者肺组织弥散功能,对于进行一氧化碳弥散测定有困难的临床中心,可以通过血气分析结合影像学检查来评估一部分低危的患者。如患者血气分析结果正常,胸部CT 提示患者肺组织除切除部分以外无明显病变,肺质地均匀且正常,且临床对进行一氧化碳的弥散心肺功能运动试验(CPET)测定有困难,则可通过此方法评估患者弥散功能。但对于血气有异常,或者影像学存在异常的患者,推荐进行一氧化碳的弥散测定来评估患者弥散功能。
推荐意见:术前动脉血气分析已不再作为肺切除手术术前功能评估的主要检测指标,在没有条件开展弥散功能检测时,动脉血气分析结合患者肺通气功能可在一定程度上评价患者肺弥散功能(推荐等级:ⅠC)。
6 特殊疾病状态患者的术前肺功能评估
6.1 双侧同期肺癌手术患者的术前肺功能评估随着 CT 体检的普及,早期肺癌的诊断时间提前,双侧同期多原发肺癌的诊断率也有所提高,此类患者的术前肺功能评估,以及切除范围决策,已成为新时期的挑战。已有相关研究显示,双侧肺癌手术的可行性,并且提示了较好的远期生存率。近期已有相关双侧同期肺癌根治性手术的报道,证实了双侧同期手术的可能性。但由于双侧胸腔完整性同时遭到破坏,以及无健侧代偿,短期内肺功能的损失高于单侧手术,其围术期并发症发生率也高于单侧手术。双侧亚肺叶切除,或单侧肺叶切除合并对侧亚肺叶切除手术,术前评估方式可沿用单侧手术评估方法。但是对双侧同期主要肺组织切除手术术前肺功能评估的方法尚无定论,我院对同期单侧肺叶切除合并对侧双段以上切除的患者进行了研究,发现此类患者围术期并发症发生率高于单侧手术患者,提示由于双侧同时胸腔完整性破坏及无健侧代偿,双侧肺切除手术术前评估需要慎重,但样本量较小,仅仅证实双侧同期手术评估需要提高推荐阈值,具体评估阈值仍需要大样本的进一步研究。
6.2 COPD 与其他弥漫性肺疾病患者术前肺功能评估
对于 COPD 患者,由于肺切除手术存在肺减容效应,应明确此类患者与正常患者间所存在的差异。Brunelli 等[61]的研究提示,PPO-FEV1<40% 预计值的 COPD 患者,经肺叶切除手术后,围术期的死亡率仅为 4.8%。Linden 等对术前 FEV1<35% 预计值(平均值为 26%)的患者进行研究,研究提示仅使用 FEV1 不能完全预测患者并发症和围术期死亡风险。以上研究者们质疑仅仅使用 FEV1 作为此类患者术前评估主要指标的准确性。一些研究也证实了,对于存在中到重度 COPD 的肺癌患者,行肿瘤根治术切除的肺实质如为 COPD 主要病变区域,由于肺减容效果的存在,患者术后肺功能损失较预计减小,甚至存在有部分提高的可能。研究同时显示,此类患者的肺减容效应是在手术后立即产生的,提示肺癌根治手术对此类患者的肺功能影响是小于无 COPD 病史的患者,对此类患者的评估应适当放宽标准,同时采用更多的检测方法再进行更为细致及准确的评估。同时应注意,对 COPD 患者进行术前呼吸道准备(使用化痰药物清理呼吸道,鼓励患者进行登楼等体能锻炼)可以明显改善患者肺功能。对于此类患者首次评估后,可通过呼吸道准备后再次进行评估,以达到手术所需肺功能标准。
对弥漫性肺疾病患者(如弥漫性大疱或者间质性肺疾病等)的术前肺功能评估,由于患者无明确病变区域或无功能区域,理论上此类患者的评估方法和普通患者相同。但根据疾病的不同特点,在术前肺功能的评估中可能需要作出一定的调整。如COPD 患者由于双上叶的病变往往大于双下叶,所以术前对上叶切除的患者可以适当放宽指征,而对于行下叶切除患者的手术应当持相对谨慎的态度。间质性肺疾病是以弥漫性肺实质、肺疱炎症和间质纤维化为病理基本病变,以活动性呼吸困难、影像学弥漫性改变、限制性通气功能障碍、弥散功能降低和低氧血症为临床表现的不同种类疾病群构成的临床-病理实体的总称。其中对特发性肺纤维化患者的术前评估应较为谨慎,此类患者的肺功能异常表现主要是用力肺活量(FVC)及 DLCO 的明显下降而 FEV1 的下降并不十分明显,故采用FEV1 作为评估指标,肺功能往往被高估,但对于此类患者的术前 FVC 指标尚无统一的阈值指标。且术后患者可能发生爆发性的病情恶化,故对此类患者的评估需要根据 FVC 和 DLCO 的指标以及切除部分及保留肺组织功能和间质性改变情况做综合考虑。因间质性肺病的患者病变较重的往往是双下叶,则对于上叶切除患者的术前评估应更为严格。同时应注意,对于特发性纤维化的患者,即便术前肺功能通气和弥散功能指标符合手术要求,也应告知患者及家属术后因肺间质性病变急性加重而导致患者死亡风险。
有相关设备支持时,可以进行肺通气/灌注显像的检测,但此检测提供的结果并非三维,不同肺叶的功能区域有明显重叠,无法明确分离,上叶切除患者的肺功能损失往往会被高估,此项检测结果仅提供一定参考价值。
6.3 合并局限性病变区域或无功能肺组织患者的术前肺功能评估
某些肺良性疾病是肺癌发生的高危因素,且肺癌也合并发生在这些基础病变区域,如 COPD、间质性肺病以及肺结核等。此外,部分肿瘤起源于近端支气管造成管腔阻塞,引起远端肺组织阻塞性肺炎或肺不张。良性疾病可能局限在一个区域,此区域肺功能一般较差。因存在局限性病变区域或者无功能局域,使有效肺单位分布不均匀情况下,术前肺功能的评估,应根据手术切除部位是否包括此类区域而定。无功能区域应该定义为,无法正常完成血-气交换的组织,这些区域可以通过肺通气/灌注显像来明确,评估每一肺组织区域的通气/灌注水平;但其空间上肺组织显像存在前后重叠,因此也可能过高或过低地评估术后肺功能。有研究显示,对于肺功能受损的肺癌患者,切除无功能区域的含瘤肺组织,并不增加术后呼吸衰竭等并发症的风险。切除无功能区域可以改善通气血流比例,对于此类患者术前的肺功能评估的阈值应适当放宽,而对于手术仅仅切除有效肺单位而未切除无功能区域的患者,术前评估应持更谨慎的态度。而对于有局限肺功能受损区域的患者术前肺功能评估,因切除部分的肺功能明显差于正常肺单位,故预计肺功能往往会被低估,更精确的肺功能评价可通过单光子发射计算机断层成像术(SPECT),SPECT可计算特定肺区域的功能情况且不受空间重叠效应的影响。
6.4 二次肺部手术前肺功能评估
二次手术的术前评估比较复杂,其主要原因在于首次手术后患者血流和通气的重新分布,导致每个肺叶的功能不再按照原来的比例分布。根据同侧和对侧再手术的不同情况,需要具体情况具体分析,必要时肺通气/灌注显像可在一定程度上明确分侧及各个部分的功能比例,从而确定预切除肺组织所占功能,再通过相应的 PPO-FEV1 和 PPODLCO的公式进行计算,将结果代入路径,从而对患者手术风险进行评估。同时根据以下所提及的一些情况也需要纳入术前评估的考虑。
影响二次肺部手术肺功能的因素包括:
(1)两次手术是否同侧。如果是同侧手术,术后肺功能降低的程度较轻;如果是对侧手术,对于肺功能的影响可能更严重,更容易发生呼吸衰竭。
(2)两次手术的间隔时间。两次手术如果间隔在 6 个月以上,那么首次手术导致的肺功能降低已基本恢复完全;两次手术如果间隔在 6 个月以内,首次手术导致的肺功能降低还有进一步恢复的可能。
(3)PPO-FEV1 和 PPO-DLCO 的计算。由于首次手术后,患者术侧胸廓缩小、胸壁肌肉损伤等因素,术侧余肺的功能可能受影响较大。不宜直接根据肺段数量计算 PPO-FEV1/PPO-DLCO,评估术后剩余的肺功能,建议采用通气血流比例检测,再结合肺通气功能计算。
推荐意见:(1)双侧同期手术由于双侧胸腔完整性同时遭到破坏,以及无健侧代偿,短期内肺功能的损失高于单侧手术,其围术并发症率也高于单侧手术(推荐等级:ⅠC)。
(2)对于弥漫性肺部疾病的患者,需要根患者实际情况,分析单个肺叶的功能情况,评估手术切除范围所占功能比例,计算预计术后肺功能,情况复杂时,需要使用肺通气/灌注显像来计算明确(推荐等级:ⅠC)。
(3)对于特发性肺纤维化患者的术前评估应较为谨慎,此类患者的肺功能异常表现主要是FVC 及 DLCO 的明显下降而FEV1 的下降并不十分明显,故采用FEV1 作为评估指标,肺功能往往被高估,但对于此类患者的术前 FVC 指标尚无统一的阈值指标(推荐等级:ⅠC)。
利益冲突:无。
参考文献:略
文章来源:中国胸心血管外科临床杂志 2020 年1 月第27 卷第1 期
www.ahyllaw.com、安徽医疗纠纷律师、合肥医疗纠纷律师、安徽医疗事故律师、合肥医疗事故律师、安徽医疗律师、合肥医疗律师、医疗事故律师、医疗纠纷律师、陈俊福律师


