中国医药教育协会胸外科专业委员会,中国胸外科肺癌联盟,浙江省医学会胸外科学分会,中国医疗保健国际交流促进会肺癌预防与控制分会
浙江大学医学院附属第一医院 胸外科(杭州 310003)
【关键词】 肺结节;三维可视化;手术规划;可切除评估
无论是我国还是全球,肺癌都是发病率和死亡率最高的肿瘤类型。手术在早中期非小细胞肺癌治疗中仍然占据核心地位。虽然肺叶切除术目前仍是早期肺癌的标准术式,但近年来亚肺切除术对于早期非小细胞肺癌的疗效及优点逐步展现。手术创伤小,恢复快,更多保留肺功能,尤其是对于心肺功能受损的特殊群体优势明显。亚肺叶切除术前评估内容包括肺结节定位、靶段血管、支气管辨认等。
肺结节在人工智能平台下的三维可视化是指用于显示、描述和解释肺结节及其周围三维空间结构和解剖形态的一种工具,它借助计算机视觉技术,对影像数据进行处理和分析计算,将肺组织、肺结节、肺内血管和支气管等结构的形态和空间分布等进行描述和解释,实现直观准确的可视化呈现,为术前精准诊断和个体化手术方案提供决策参考。
目前国内外已存在多种三维重建工具,在肝胆胰腺疾病中的应用已有相关专家共识。为了规范肺结节临床诊治中三维可视化技术的应用,中国医药教育协会胸外科专业委员会、中国胸外科肺癌联盟、浙江省医学会胸外科学分会、中国医疗保健国际交流促进会肺癌预防与控制分会联合发起并制定相关共识。
本共识的推荐级别为:1A 级:基于高水平证据,专家组有统一认识;1B 级:基于高水平证据,专家组有小的争议;2A 级:基于低水平证据,专家组有统一认识;2B 级:基于低水平证据,专家组无统一认识,但争议不大;3 级:专家组存在较大争议。
1 肺结节术前影像学诊断和评估
共识级别:2A 级。
肺结节的影像学诊断方法主要包括胸部 X 线和 CT 等检查,但这些检查手段存在以下不足:(1)只能提供二维影像;(2)无法立体显示肺结节与肺动脉、静脉和支气管的关系;(3)无法将肺、肺结节、肺内血管和支气管赋以不同颜色、不同透明度进行展示;(4)需由影像专业人员协助分析影像;(5)无法配合术前规划进行仿真手术。
近年来,数字医学技术和精准诊疗模式不断发展,人工智能三维可视化技术在医疗领域的发展取得了巨大的进步,比传统的二维影像更加直观精确,在术前可切除性评估和手术方案制定等方面发挥了重要作用。
建议:对已经行 X 线或 CT 等影像学技术发现肺结节并决定行手术治疗的患者,若结节与累及的血管、支气管或肺段无法准确评估,建议应用人工智能三维可视化技术进行进一步精准评估。
2 肺结节薄层增强 CT 数据采集
共识级别:2A 级
常规采集肺部薄层增强 CT 影像数据,扫描结束后将影像数据传至处理工作站,进行刻盘存储。
数据采集基本要求:(1)三期增强扫描数据(平扫期、动脉期、静脉期);(2)层厚≤1 mm;(3)标准 DICOM 格式;(4)无伪影、无颗粒状、无锯齿状,显影清晰。
数据采集其他要求:(1)患者的全部 CT 数据;(2)患者的病例病史。
建议:胸外科应与放射科互相配合,根据结节的性质、大小、可能有密切关系的血管、支气管的异同,综合本院 CT 实际情况,优化扫描参数,以期获得高质量三维 CT 图像数据。
3 肺结节在人工智能平台下的三维可视化模型的建立
共识级别:1B 级。
3.1 CT 数据的分析和三维可视化
将采集到的薄层增强 CT 影像数据导入精准手术 3D 分析规划系统,借助人工智能手段,进行图像分析和重建。通过调节透明度可同时显示肺、肺结节、肺动脉、肺静脉和支气管,了解肺动脉、肺静脉、支气管的走行和变异,通过对模型的放大、缩小、旋转观察,能从多角度更清晰地了解各结构之间的空间位置关系。
建议:对 CT 数据进行人工智能三维可视化重建以实现精准手术,三维重建可以帮助术者对结节、血管、支气管、肺段等解剖结构的空间位置关系有更好的理解和对策。
3.2 三维可视化肺段支气管分型
根据肺段支气管的分布,将肺脏分为左、右两肺。其中右肺分为 3 叶 10 段,左肺分为 2 叶 8 段。每个肺叶按肺段支气管分支数目进行分型,见图 1、图 2。
肺段分型可出现一定概率的解剖变异。对于左肺上叶主要分型:Ⅰ型:左肺上叶分为尖后支、前支、上舌支、下舌支;Ⅱ型:左肺上叶分为尖支、后支、前支、上舌支、下舌支。
对于左肺下叶主要分型:Ⅰ型:左肺下叶分为背支、内前基底支、外基底支、后基底支;Ⅱ型:左肺下叶分为背支、内前基底支、外后基底支。
对于右肺上叶主要分型:Ⅰ型:右肺上叶分为尖支、后支、前支;Ⅱ型:右肺上叶分为尖后支、前支;Ⅲ型:右肺上叶分为尖支、后支、前支、亚前支。
对于右肺中叶主要分型:Ⅰ型:右肺中叶分为内侧支、外侧支。
对于右肺下叶主要分型:Ⅰ型:右肺下叶分为背支、外基底支、前基底支、内基底支、后基底支;Ⅱ型:右肺下叶分为背支、内基底支、内前外基底支、后基底支;
建议:对于拟行手术的肺结节患者,术前采用人工智能三维可视化技术进行支气管重建,可明确结节与支气管的解剖毗邻关系及支气管可能存在的解剖变异。
3.3 三维可视化肺动脉分型
根据肺动脉的分布,将肺动脉分为左肺动脉和右肺动脉,再按每个肺叶内肺段动脉分支数目进行分型,见图 3、图 4。清晰准确的动脉重建有助于临床医生对动脉走行有更加客观的认识,减少术中血管损伤,保证手术安全。
对于左肺上叶动脉主要分型:由左肺动脉发出,其分支数为 2~6 支,以 4 支为最多,其次为 3支;左肺动脉第一分支分布至前段及尖后段占多数,其次是前段,单独分布至尖后段的很少;左肺上叶的舌段动脉有一支型和两支型,其中,一支型的占多数。
对于左肺下叶动脉:左肺下叶的背段动脉可分为一支型,二支型、三支型;左肺下叶基底段动脉以 A7+8,A9+10 为最多;基底段动脉与舌段动脉共干。
对于右肺上叶动脉:右肺上叶的动脉由右肺动脉分出,其分支数为 1~4 支,以 2 支为最多,3支次之,1 支和 4 支最少。
对于右肺中叶动脉:右肺中叶的动脉,其分支数为 1~3 支,二支的最多,一支的次之,三支的最少。右肺中叶的动脉分支与下叶的动脉分支共干。
对于右肺下叶动脉:右肺下叶的背段动脉,有一支型或二支型;右肺下叶的背段动脉与上叶的动脉分支共干;右肺下叶基底段动脉以 A7+8、A9+10、A7、A8 为最多。
建议:对于拟行手术的肺结节患者,术前采用人工智能三维可视化技术进行肺动脉重建,可明确结节与肺动脉的毗邻关系及肺动脉的解剖变异,了解手术靶区的血供情况,实施精准解剖性手术。
3.4 三维可视化肺静脉分型
按照肺静脉开口数目及副肺静脉情况,可将肺静脉分为 4 种类型:标准型、肺静脉共同开口型、副肺静脉型、混合变异型。肺静脉示意图见图 5。
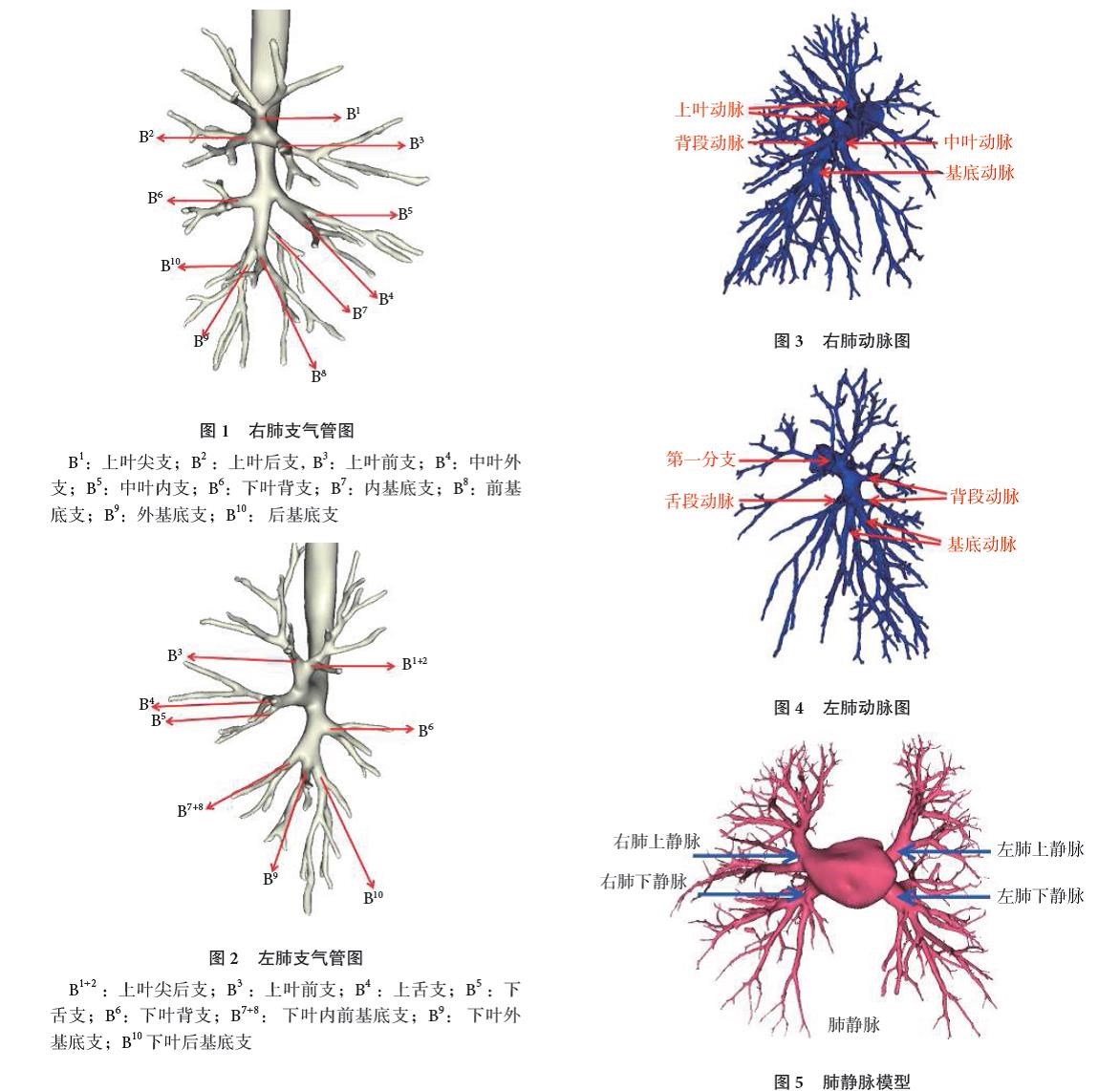
(1)标准型:4 个肺静脉开口,4 条肺静脉,左右各 2 条。(2)肺静脉共同开口型:在标准型的基础上形成了肺静脉共同开口,表现为肺静脉开口 2个或 3 个,而肺静脉仍为 4 条,左右各 2 条。根据共同开口的位置又可以分为 3 个亚型,即右侧共同开口型、左侧共同开口型、双侧共同开口型。(3)副肺静脉型:在标准型的基础上出现了副肺静脉,表现为肺静脉开口 5 个或更多,肺静脉为 5 条或更多,其中左右各 2 条肺静脉,其余均为副肺静脉。又根据副肺静脉出现的位置分为 3 个亚型,即右侧副肺静脉型、左侧副肺静脉型、最上肺静脉型。(4)混合变异型:肺静脉共同开口与副肺静脉同时存在,一侧出现共同开口,2 条肺静脉,另一侧除去2 条肺静脉外出现副肺静脉。
高质量的三维重建技术可清晰地显示肺内动脉、静脉和支气管的变异,对于微创时代胸外科手术的安全性提供了有力保障。
建议:对于拟行手术的肺结节患者,术前采用人工智能三维可视化技术进行肺静脉重建可明确结节与肺静脉的解剖毗邻关系及肺静脉的解剖变异,规避静脉误断,保证手术安全、精准。
3.5 三维可视化个体化肺分段
随着精准外科理念的深入,近年来各类肺段切除乃至亚肺段切除术式快速发展,对基于肺部支气管走行的肺段和亚肺段三维重建提出了更高的要求,理论上肺段支气管分支与肺动脉分支伴行,肺静脉分支走行于相邻肺段之间,每个肺段构成了肺的形态学和功能学上的基本单位。三维可视化工具可以对正常及变异肺段进行基于个体化数据的重建,但在段间界面的显示和确定方面尚有不足。新一代的人工智能技术,提供了智能化并且实时交互的全定量、定性分析工具(IQQA 技术),可基于患者个体化气管的空间分布,对正常及变异肺段乃至亚肺段进行重建,准确使用全面定量化的三维影像展现患者真实的支气管和血管拓扑关系,具有很好的临床实用性。全定量三维重建后的肺段显示具有良好的视觉效果,见图 6、图 7。
建议:肺段切除术患者术前应进行个体化人工智能三维可视化评估,明确肺结节所在肺段或亚段,实现精准定位和精准手术,在保证肿瘤切缘安全的同时最大限度保留肺功能。
4 术前评估
共识级别:2A 级。
肺结节影像数据经过三维可视化处理和个体化肺分段后,可以清晰地显示肺结节的位置、大小、形态和分布,然后对肺动脉、肺静脉和支气管的变异进行分析,对肺结节与肺动脉、肺结节与肺静脉和支气管的解剖关系进行风险评估。
建议:对于发现肺结节拟行手术的患者,建议术前采用人工智能三维可视化评估,全面评估手术风险,保证手术安全。
5 三维可视化指导精准手术术前规划
共识级别:2A 级。
传统胸部 X 线片、CT 等难以分辨肺静脉、肺动脉和支气管的变异,而三维可视化技术则可以直观地将肺静脉、肺动脉、支气管的个体化特异性表现出来。
肺段切除术前规划流程:(1)肺部薄层增强CT 扫描(层厚≤1 mm);(2)数据导入精准手术3D 分析规划系统进行三维可视化和个体化肺分段;(3)定位结节所在位置(肺段或肺亚段);(4)分析肺段三大结构即支气管、肺动脉、肺静脉;(5)模拟靶区肺段切除范围;(6)根据病例的具体解剖特点制定手术计划,制定段支气管、动脉、静脉的处理顺序。肺结节经过三维重建之后可以清晰地显示与动脉、静脉、支气管和肺段的解剖关系,见图 8。
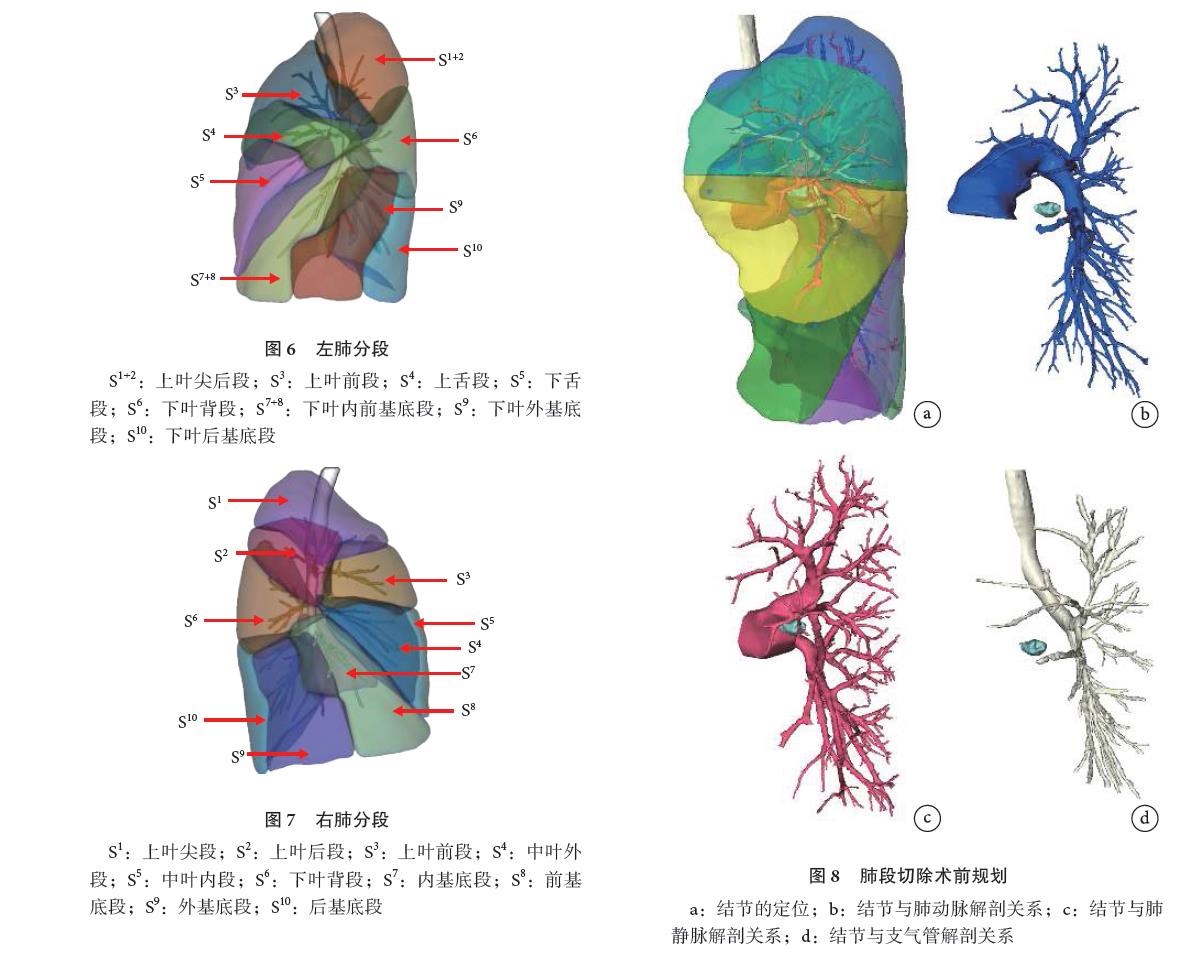
5.1 结节定位
对于肺结节的定位,以往采用以下几种:(1)胸腔镜下直接观察法定位;(2)术中手指或器械触摸法定位;(3)亚甲兰定位;(4)经皮肺穿刺放置微弹簧圈进行定位;(5)经皮肺穿刺 Hook-wire 定位;(6)电磁导航支气管镜技术定位;(7)荧光定位;(8)术中用胸内超声探头进行肺内结节定位;(9)其他,如改良的 Hook-wire 和弹簧圈定位等。
现在,术前使用计算机技术对薄层增强 CT 影像进行三维可视化,实现了从二维到三维的转换,可以全面、直观、准确、客观地展示肺结节情况,而且安全、无创,为解决传统结节探查、触摸、确认困难提供了一个“智能定位地图”。
通过三维可视化可以辨别结节的位置,分析结节与肺动脉、肺静脉和支气管的解剖关系,明晰术中解剖可能存在变异,进一步接近术中的实际解剖情况,精准定位肺结节所在的肺段和/或亚段,从而改变肺叶/肺段切除方式,最大程度保存健康的肺组织,提高手术的安全性和准确性。通过人工智能三维可视化在术前进行手术模拟,可缩短术中手术时间,减小患者损伤。
建议:术前采用人工智能三维可视化工具对肺结节进行定位。
5.2 楔形切除术前规划
肺楔形切除术多用于局限性边缘性良性结节,切除肺组织不宜过多、过深,否则易伤及较大血管或支气管,引起大出血或支气管胸膜瘘。肺楔形切除时,肺实质内肺结节的定位困难,而术前对薄层增强 CT 影像进行三维可视化,很方便、直观地定位肺结节位置,测量肺结节距离大的动脉血管、静脉血管和支气管的长度,选择合理的切除范围。
建议:建议行肺楔形切除的患者术前采用人工智能三维可视化工具进行术前规划,选择科学合理的个体化切除方案。
5.3 肺段切除术前规划
为精准切除结节所在的肺段或亚段,术前应进行三维可视化和肺分段或肺分亚段,定位结节所在的肺段或亚段,对于胸腔镜和机器人肺段切除手术均可提供帮助。依据三维可视化和肺分段或肺分亚段结果,明确病例解剖特点:(1)肺段是否与标准解剖一致;(2)靶肺段或亚段动脉是否存在变异(包括返支、升支、共干等);(3)靶肺段或亚段支气管是否存在变异;(4)靶肺段或亚段静脉是否存在变异。根据病例的具体解剖特点规划手术流程:(1)根据结节所在的肺段或肺亚段,来确定预切除范围,是肺段切除还是联合肺段切除;(2)靶肺段动脉的处理,离断靶段动脉分支;(3)靶肺段支气管的处理,离断靶段支气管分支;(4)靶肺段肺静脉的处理,离断段内肺静脉,保留段间静脉。
建议:行肺段切除的患者术前采用人工智能三维可视化工具进行确切的术前规划,保障精准肺段手术的实施。
5.4 二次手术术前规划
因患者已做过一次手术,剩余肺叶的充分膨胀所致原有解剖结构空间相互位置的改变或者回流静脉粗细的改变,靶肺段或亚段动脉、静脉、支气管变异,从而造成了二次手术术中辨认困难,如行同侧二次手术,更需对肺内血管、支气管、肺结节的大小、肺结节的数量进行分析、评估。同样,在术前需进行薄层增强 CT 的三维可视化和肺分段或肺分亚段,定位结节所在的肺段或亚段。依据三维可视化和肺分段或肺分亚段结果,明确患者解剖特点:(1)肺段或肺分亚段是否与标准解剖一致;(2)靶肺段或亚段动脉、静脉、支气管是否存在变异。根据患者的具体解剖特点规划手术流程:(1)根据结节所在的肺段或肺亚段,来确定预切除范围;(2)靶肺段动脉、静脉和支气管的处理,哪些该离断,哪些该保留。
建议:行二次手术的患者术前采用人工智能三维可视化工具进行术前规划,尤其是同侧二次手术的患者,三维重建更具优势。
6 结语
三维可视化的技术优势在肺结节的诊断中愈加明显,对已用传统胸部 X 线片、CT 等影像学技术初步诊断为肺结节且需要接受肺切除术的患者,建议对进行肺部目标病灶的三维可视化分析,有条件的单位还可结合肺脏 3D 打印、混合现实 QMR技术进行评估,使人工智能平台下的三维可视化技术为术前精确诊断、术中精准手术、患者快速康复和最大获益提供更大的支持保障。
利益冲突:无。
撰稿专家:支修益(首都医科大学宣武医院胸外科)、胡坚(浙江大学医学院附属第一医院胸外科)、刘伦旭(四川大学华西医院胸外科)、蔡开灿(南方医科大学南方医院胸外科)
执笔专家:徐金明(浙江大学医学院附属第一医院胸外科)、汪路明(浙江大学医学院附属第一医院胸外科)、杜澄利(浙江大学医学院附属第一医院胸外科)
审稿专家组名单(按姓氏拼音排序):陈椿(福建医科大学附属协和医院胸外科)、陈克能(北京大学肿瘤医院胸外科)陈龙奇(四川大学华西医院胸外科)、陈铭伍(广西医科大学第一附属医院心胸外科)、方文涛(上海交通大学附属胸科医院胸外科)、付军科(西安交通大学医学院第一附属医院胸外科)、付向宁(华中科技大学同济医学院附属同济医院胸外科)、高树庚(中国医学科学院肿瘤医院胸外科)、葛棣(复旦大学附属中山医院胸外科)、郭占林(内蒙古医科大学附属医院胸外科)、何建行(广州医科大学附属第一医院胸外科)、矫文捷(青岛大学附属医院胸外科)、李小飞(空军军医大学第二附属医院胸外科)、李印(中国医学科学院肿瘤医院胸外科)、刘建阳(吉林省肿瘤医院胸外科)、刘俊峰(河北医科大学第四医院胸外科)柳阳春、(江西省人民医院心胸外科)、鲁继斌(中国医科大学附属盛京医院胸外科)、马海涛(苏州大学附属第一医院胸外科)、尼平(西藏自治区人民医院心胸外科)、孙大强(天津市胸科医院胸外科)、孙伟(新疆医科大学附属肿瘤医院胸外科)、许林(江苏省肿瘤医院胸外科)、徐美青(安徽医科大学附属省立医院胸外科)、张春芳(中南大学湘雅医院胸外科)、张兰军(中山大学附属肿瘤医院胸外科)、张临友(哈尔滨医科大学附属第二医院胸外科)、朱成楚(温州医科大学附属台州医院心胸外科)、朱余明(同济大学附属上海市肺科医院胸外科)
参考文献:略
文章来源:中国胸心血管外科临床杂志2019年12月第26卷第12期
www.ahyllaw.com、安徽医疗纠纷律师、合肥医疗纠纷律师、安徽医疗事故律师、合肥医疗事故律师、安徽医疗律师、合肥医疗律师、医疗事故律师、医疗纠纷律师、陈俊福律师


