王乔宇,武明芬,柳 鑫,王晓岩,陈耀龙,赵志刚
摘要: 静脉血栓栓塞症近年来越来越引起医学界的广泛关注。本指南依照世界卫生组织( WHO) 指南制作标准进行制定,证据与推荐意见的评价方法用评估建议的评级、发展和评价( GRADE) 分级。为更好地指导我国医师、药师的临床实践,本指南系统评价了深静脉血栓防治中抗凝药物使用中的循证证据,针对不同科室抗凝药物的选用和药学监护、抗凝药物过量的处理等共计 30 个临床问题从药师的角度给出推荐意见,进一步规范我国静脉血栓栓塞防治中抗凝药物的合理使用。
关键词:静脉血栓栓塞;深静脉血栓;抗凝药物;药学监护;指南
静脉血栓栓塞症(venous thromboembolism,VTE)包括深静脉血栓形成(deep vein thrombosis,DVT)与肺栓塞 (pulmonary embolism,PE)。VTE 是住院患者常见并发症及死亡原因,具有发生率高、病死率高和住院费用高的特点。VTE 的防治与管理在国际医学界一直备受关注,国外推出多项 VTE 预防指南,我国也制订了多个临床专业的的 VTE 防治指南,开始积极推进 VTE的防治。但由于我国在 VTE 诊治研究方面起步较晚,目前仍有相当一部分医务人员对 VTE 的预防和治疗认识不足,VTE 预防和治疗药物选择、药学监护仍存在诸多问题和不规范,迫切需要出台全面、针对临床问题的防治指南,提升我国 VTE 防治中抗凝药物的合理使用水平。本指南结合近年来国内外发表的相关指南和临床研究文献,系统评价了 VTE 防治过程中,抗凝药物在不同科室、不同疾病人群中选用和药学监护的循证医学证据,参考世界卫生组织(World Health rganization,WHO)指南的制定原则形成本指南。
1 指南制定工作组织管理和形成过程
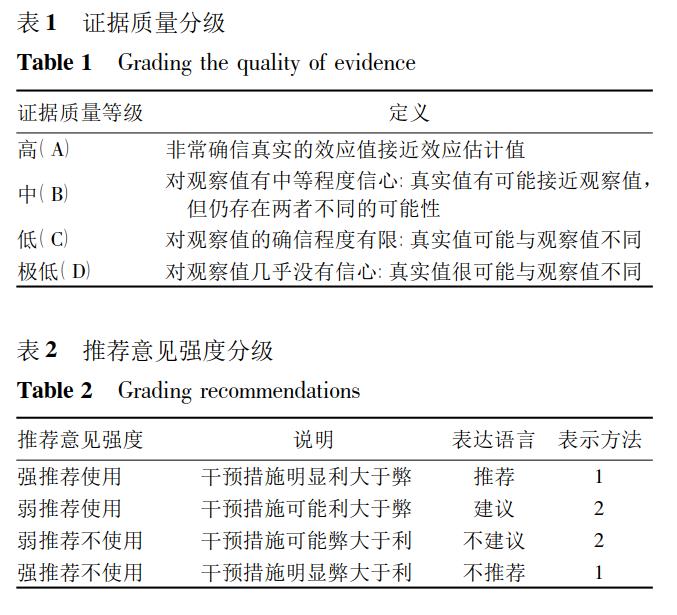
本指南证据质量与推荐强度分级用评估建议的评级、发展和评价 ( grading of recommendations sessment,development and evaluation,GRADE)分级系统,相应的证据质量分级与推荐强度分级见表 1,2。
指南制定的基本步骤遵循《世界卫生组织指南制定手册》。本指南已在国际实践指南注册平台进行注册(注册号:IPGRP - 2018CN041)。指南制定团队由指导组、专家组、循证秘书组以及外审组构成。指导组和专家组包含内科、外科、妇产科、药学、循证医学等多领域专家。指导组主要职责是确定指南主题和范围,组建其他小组,管理相关人员的利益声明并批准指南计划书,最终批准推荐意见与指南全文。专家组主要确定指南的临床问题纳入文献的人群、干预措施、对照和结局(population,interventions,comparisons,outcomes,PICO),并为初稿的制定提供意见;对于没有确切证据的问题或争议问题通过德尔菲法达成推荐的共识意见。指南纳入的临床问题最初由文献调研分析提出,经专家德尔菲法打分后最终确定纳入本指南的临床问题。循证秘书组负责系统地检索相关临床问题已有的循证证据,对于近 3 年的高质量系统评价直接采纳,否则对系统评价的文献纳入进行更新,完成系统评价、证据分级,撰写证据总结表等,部分临床问题参考目前已有的临床指南。此外秘书组详细记录指南制定的过程,进行数据收集与分析,撰写指南初稿。经 3 轮德尔菲法的线上专家工作会议确定了最终的推荐意见与推荐强度。外审组主要由为直接参与指南相关工作的专家组成,其主要完成对指南全文的审阅和修订。本指南由中国健康促进基金会医药知识管理(MKM)专项基金进行支持,工作组成员均已签署利益声明表,不存在相关利益冲突。
经专家德尔菲法投票,本指南拟纳入临床问题共41 项。将纳入的临床问题按照 PICO 原则在相关中英文数据库 (万方、维普、CNKI、Pubmed、Web of Science、EmBase、Cochrane Library)进行检索,纳入系统评价、Meta 分析、网状 Meta 分析、临床指南以及相关原始研究。每项临床问题检索策略经指南指导组进行审阅。用评估系统评价的测量工具(Assessing the Methodological Quality of Systematic Reviews,AMSTAR)对纳入的系统评价等进行质量评估,用Cochrane偏倚风险评价工具、文献质量评价量表(Newcastle-Ottawa Scale,NOS)对相应的原始研究进行质量评价。由于部分临床问题原始研究缺失或极少且质量低,最终本指南针对 30 项临床问题提供推荐意见。
2 指南涉及的临床问题与推荐意见
针对30 项临床问题,形成相应的 PICO,通过证据评价形成证据等级,使用改良的德尔菲法给出推荐意见以及对应的推荐强度。
PICO 1 医院内成立 VTE 防治管理团队可降低 VTE发生率?
纳入的中文文献 7 篇和英文文献 2 篇均为回顾性的观察性研究。对照组为成立 VTE 防治管理团队前,试验组为成立 VTE 防治管理团队后。荟萃分析结果显示,成立 VTE 防治管理团队后,VTE 发生率出现显著下降 (P<0. 0001,OR:0. 23,95% CI:0. 09~0. 64)。通过在院内实施 VTE 防治管理措施,建立规范的 VTE 管理制度和组织构架,制定完善的住院患者 VTE 风险评估体系和防治方案,采取全员培训、重点科室试行直至全面推广的实施步骤,建立起医院规范化 VTE 防治与管理体系,并通过多学科协作(医、药、护)的工作模式深入开展院内 VTE 防治工作,取得了良好效果。
推荐意见 推荐各医疗机构在院内成立 VTE 防治管理团队,可显著降低院内 VTE 发生率(1C)。
PICO 2 药师参与 VTE 管理并明确职责可降低 VTE发生率?
纳入的中文文献 3 篇和英文文献 3篇均为基于时间序列的前后对照研究,通过药师参与管理,可有效降低患者 VTE 的发生率、复发率和出血事件的发生率,并提高 INR 达标率等。荟萃分析结果提示,药师参与 VTE 管理可有效降低患者 VTE的发生率 ( P<0. 05,OR:0. 25,95% CI:0. 12~0. 54)。因此,将药师纳入 VTE 防治管理团队十分必要,药师的职责包括并不限于:评估患者深静脉血栓的风险、对患者 VTE 预防措施进行宣教、及时调整VTE 预防方案等。
推荐意见 推荐医疗机构将药师纳入 VTE 防治管理团队,以降低患者 VTE 发生率(1C)。
PICO 3 肝功能不全的患者预防 VTE 抗凝药物应如何使用?
针对肝功能不全患者 VTE 预防纳入 1 项系统评价,其中纳入 3 项肝素的回顾性对照研究,荟萃结果显示,使用肝素与不使用肝素比较,VTE 发生率差异无统计学意义(P>0. 05,OR:1. 65,95% CI:0. 36~7. 54),出血风险差异也无统计学意义(P>0. 05,OR:0. 87,95% CI:0. 34~2. 18)。在一项非盲法、单中心、针对晚期肝硬化患者的 RCT 研究中,依诺肝素组和无预防的对照组出血事件发生率未发现显著性差异。存在下肢深静脉血栓风险的患者相较于未进行预防组,依诺肝素预防组的患者在48 周(P<0. 05)与 96 周(P<0. 01)均未出现下肢深静脉血栓,且患者肝硬化失代偿发生率显著低于对照组(12% vs 59%)。
新型口服抗凝药 ( novel oral anticoagulants,NOACs)针对肝功能不全调整剂量的原始研究较少。
建议 NOACs 的使用参照药品说明书根据肝功能调整剂量。其中,利伐沙班在 Child-Pugh B/C 级患者中禁用;阿哌沙班、艾多沙班在严重肝功能损害时禁用;阿哌沙班在中度肝损害时,尚无用药经验,故不建议使用;艾多沙班在轻中度肝损害时应慎用。达比加群在中度肝损害时无需调整剂量。华法林(VKA)原研药品说明书中未限制肝功能不全患者用药,但国产药品均将肝功能不全列为 VKA 的禁忌症。
推荐意见 (1)对于肝功能不全尤其是肝硬化的患者,推荐首选低分子肝素预防 VTE,剂量为标准剂量(1B);(2)建议使用 VKA 及 NOACs 用于肝功能不全患者时,应依照说明书使用,并注意监测肝功能和凝血指标(2C)。
PICO 4 肾功能损害的患者预防 VTE 抗凝药物应如何使用?
文献检索发现,目前没有针对患者肾功能受损时VTE 防治抗凝药物剂量调整的相关研究。肾功能受损时用药剂量调整主要来源于国内外药品说明书。
(1)肝素类药物肾功能损害时的剂量调整:患者内生肌酐清除率(endogenous creatinine clearance rate,Ccr)在 50~70 mL·min-1 时:使用普通肝素、依诺肝素、那曲肝素或达肝素时均无需调整剂量;Ccr 在 30~50 mL·min-1 时:使用普通肝素、依诺肝素或达肝素时无需调整剂量,那曲肝素需要减少25%~33% 的正常剂量;当 Ccr<30 mL·min-1 时:普通肝素无须调整剂量,依诺肝素推荐 2000 AxaIU,qd;那曲肝素不推荐使用,使用达肝素 3~4 次后应监测抗 Xa 水平(0. 5~1. 5 U·mL-1 )。(2)NOACs 肾功能损害时的剂量调整:患者内生肌酐清除率(Ccr) 在50~70mL·min-1 时:使用 NOACs 均无需调整剂量;Ccr 在30~50 mL·min-1 时:达比加群需要减量至150 mg qd或 75 mg bid,艾多沙班应减量至 30 mg·d-1 ,利伐沙班、阿哌沙班、贝曲沙班无须调整剂量;当 Ccr < 30mL·min-1 时:达比加群禁用,利伐沙班应避免使用,艾多沙班不推荐使用,阿派沙班慎用,贝曲沙班应在首日给予80 mg,随后40 mg·d-1 。此外,目前达比加群针对肾功能不全时的剂量调整国际标准尚不统一,达比加群原研药中度肾功能不全无需调整剂量,而国产药品需要减量至 150 mg·d-1 。欧盟 SPC(Summary of Product Characteristics)建议:中度肾功能不全患者预防 VTE 应减少剂量至 150 mg qd。美国 FDA 说明书:中度肾功能不全患者应减少剂量至 75 mg qd。(3)其他抗凝药物肾功能损害时的剂量调整:患者 Ccr在50~70 mL·min-1 时:华法林、比伐卢定、磺达肝癸钠和阿加曲班均无须调整剂量;Ccr 在30~50mL·min-1 时:华法林、比伐卢定和阿加曲班均无须调整剂量,磺达肝癸钠 1. 5 mg,qd;当 Ccr<30mL·min-1 时:华法林和阿加曲班无须调整。磺达肝癸钠禁用(Ccr <20 mL·min-1 ),比伐卢定在使用时应降低输液速度至 1 mg·kg-1·h-1 ,并监测凝血。此外,国产华法林在中毒肾功能不全时应禁用。
推荐意见 推荐参照药品说明书,根据肌酸酐清除率调整抗凝药物剂量。
PICO 5:血小板计数减少或功能异常的患者预防VTE 抗凝药物如何使用?
引起血小板异常的疾病包括癌症相关的血小板减少症、原发性、免疫性血小板减少症、脾切除和血小板减少性紫癜等。对于癌症相关的血小板减少症(cancer -associated thrombocytopenia,CAT)患者,VTE的风险不会随着血小板的降低而降低,血小板减少并未显示出对复发的 VTE 有任何保护作用,但与出血率的增加有关。血小板计数(PLT) < 50×10 9/L 与PLT>50×10 9 /L 的患者相比,VTE 的发生率与复发率都显著升高。约 13%使用抗凝药物的 CAT 患者出现大出血事件。
当血小板计数>50×10 9 /L 时,给予全剂量抗凝药物似乎是安全的。而 PLT <50×10 9 /L 时,出血风险似乎增加。NCCN 指南指出,当 PLT<50×10 9 /L 时是 VTE 预防用药的相对禁忌症。临床上应评估患者栓塞与出血风险。纳入包含 12 项回顾性研究的系统评价,研究对象为患有癌症相关的血小板减少症的患者 121 例,其中 27%的患者最终经历了复发性的 VTE。系统评价结果表明:CAT 患者的抗凝治疗目前仍然存在争议。部分研究建议使用低剂量的 LWMH,部分研究建议输注血小板联合全剂量低分子肝素抗凝。两种策略并未分出优劣。研究并未报告低分子肝素的使用疗程。目前尚无使用 NOACs 对CAT 患者进行预防的相关循证证据。
推荐意见 对于癌症相关的血小板减少的患者,高血栓风险的患者,建议根据患者血小板计数水平选择低剂量低分子肝素(PLT <50 ×10 9 /L)或正常剂量低分子肝素(PLT >50 ×10 9 /L)联合血小板输注预防VTE(2C)。
PICO 6:心衰患者预防 VTE 抗凝药物方案如何调整?
根据 NYHA 心力衰竭分级,病情从轻到重分为Ⅰ、Ⅱ、Ⅲ和Ⅳ级。充血性心衰与 VTE 的关联体现在患者高龄、心输出量减少、长期制动、下肢远端水肿和增大远端深静脉栓塞的风险;慢性缺氧引起肺部血管收缩,也会造成肺栓塞风险增加;急性加重期的心衰可以激活血栓素相关通路,引起炎症、内皮细胞功能障碍和静脉血栓形成。目前静脉血栓、肺栓塞和充血性心衰的关系逐步被确认,心衰患者具有更高的VTE 发生率、复发率以及死亡率,因此临床高度重视该类患者的 VTE 预防;但是很少有研究直接评估心衰患者的 VTE 预防方案,纳入的结果多为大型临床试验的亚组分析,或是对临床结果的分层研究。目前尚无研究支持使用 VKA 在心衰患者中预防 VTE。一项前瞻性队列研究发现,严重左心功能不全的患者对 VKA 所需剂量偏低(P < 0. 001),但出血风险并没有增加。
推荐意见 对于住院 3 d 以上的Ⅲ ~ Ⅳ级心衰患者、或心衰伴制动 3 d 以上、或心衰伴有严重感染、抑或是 VTE 评分高危/极高危的患者无抗凝禁忌时,应预防性抗凝,预防使用抗凝药物方案,见表 3。

PICO 7:华法林与 NOACs 之间应如何转换与桥接?
华法林与 NOACs 之间的转换与桥接方案主要来自药品说明书,见表 4。
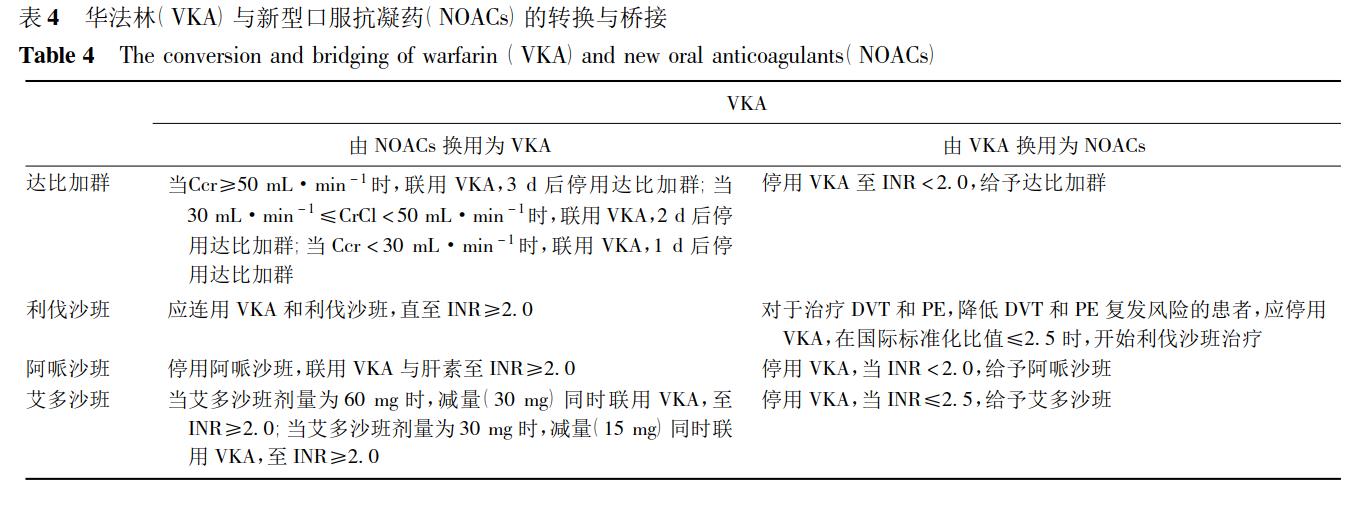
推荐意见 建议根据上表进行 NOACs 与 VKA的转换与桥接。
PICO 8:肝素类与华法林之间应如何转换与桥接?
肝素类药物与 VKA 之间的转换与桥接主要来源于药品说明书与国内外指南,该临床问题不提供证据等级与推荐强度。(1) 急性期 DVT 介入术后的患者,推荐使用沙班类等 NOACs,也可以使用低分子肝素皮下注射,q12h,5~7 d;用药第 4 天开始口服VKA 至 6 个月。(2)在 VTE 急性期肝素与 VKA 应该桥接。应用肝素超过 5 d,INR 在治疗范围即可停用肝素;也有建议称要维持 INR 治疗范围 2 d 以上才予以停用肝素。开始低分子肝素、磺达肝癸钠或普通肝素治疗至少5 d,直到 INR 大于2 且维持24 h 以上。(3)外科围手术期,一般在停用 VKA 后第 2 天启用普通肝素或低分子肝素治疗,术前4 ~6 h 停用普通肝素,术前 20 ~24 h 停用低分子肝素。术后根据不同出血风险选择 24 ~72 h 开始使用普通肝素或低分子肝素,对于出血风险高的大手术,普通肝素或低分子肝素在术后 48~72 h 恢复。术后在止血彻底的前提下,建议 12~24 h 恢复 VKA 治疗(常用剂量,一般在手术当晚或第 2 天),当 INR >2 时,停用肝素类药物。在高风险手术前停用 VKA 5 d,并且当 INR 值降到治疗有效范围以下,以治疗剂量开始低分子肝素桥接治疗。(4)肿瘤相关的 VTE 如果采用 VKA 作为长期用药,在转换时应该有至少 5 ~7 d 的过渡期,在此期间,联合使用注射用抗凝药物(如普通肝素、低分子肝素或磺达肝癸钠)与 VKA,直至 INR≥2,然后停用注射用抗凝药物。
PICO 9:老年患者防治 VTE 抗凝药物的选用?
老年深静脉血栓患者接受任意方式的静脉血栓预防措施的预防率不到 50%。复杂合并症、多种 VTE危险因素和非典型表现使老年患者特别容易发生DVT。住院频繁的老年患者 VTE 预防率相当低。许多研究已经确定年龄是 VKA 治疗期间发生大出血事件的独立危险因素。老年人抗凝药物使用注意事项如下,未形成推荐意见。
VKA (1)治疗老年人下肢静脉血栓,治疗开始时,给予 LMWH 5000 U 皮下注射,1 次/12 h,连用 10d,与 VKA 重叠后替换为 VKA,VKA 0. 83~1. 25 mg(初始剂量 0. 83 mg,1 次/天)给药,INR 达标后停用LWMH,口服 3 个月。(2)对高龄住院 VTE 患者,临床需关注其全身情况,并针对性采取安全剂量与除药物外的其他有效措施,针对消化道出血患者可考虑置入静脉滤器,同时行 LMWH 治疗,禁止服用 VKA。(3)老年患者对VKA的敏感性增加,适度抗凝(1.6~2.5,INR)似乎是最安全和最有效的,通常用药时需要减少治疗剂量和持续时间。建议每两个月监测一次 INR。
肝素类 (1)非大面积肺血栓栓塞(PTE)和部分次大面积 PTE 患者适于用 LMWH 抗凝;对于需迅速扭转病情、高出血风险、过度肥胖或严重肾功能不全的老年 PTE 患者推荐普通肝素(UFH)抗凝,而血小板减少或有肝素诱导的血小板减少史的 PTE 患者应使用非肝素类药物治疗。(2)VTE 的预防:LMWH 和低剂量 UFH 作为预防的首选方案,老年人不改变剂量和疗程。静脉 UFH 相关的出血风险<3%,而且出血发生率随着肝素剂量和年龄(>70 岁)的增长而增加。(3)老年人近端 DVT 的长期治疗中,固定剂量依诺肝素与口服抗凝药物相比,疗效相似,前者可能有更少的出血并发症。(4)需要长期 LMWH 抗凝治疗的老年人,可能会增加骨折的风险。因此对此类患者,应考虑定期监测骨密度,同时补充钙和维生素 D。
新型口服抗凝药 (1)急性 VTE 患者可选择利伐沙班、阿哌沙班、艾多沙班的单药治疗,不需要初始肝素治疗。使用 NOACs 可以固定剂量给药,无需频繁的实验室监测,且不用频繁调整剂量。(2)老年人髋部骨折术前口服利伐沙班能有效预防术前下肢DVT 的形成,并不会明显增加术中及术后手术部位的出血量,对其他部位的出血也无促进作用。(3)对于糖尿病老年患者,阿哌沙班预防老年合并糖尿病患者髋关节置换术后静脉血栓栓塞优于依诺肝素,且不增加出血风险,不影响空腹血糖。(4)对于年龄大于 75岁且伴有肾功能异常的老年患者可选择利伐沙班和阿哌沙班,尤其是对于低体重的老年女性患者。NOACs与 VKA 相比,VTE 复发和大出血风险可能显著降低。
PICO 10:妊娠期妇女预防 VTE 抗凝药物方案的选用?
妊娠为 VTE 发生一项危险因素,对于 VTE 风险较高的妊娠妇女,建议进行药物预防。目前 NOACs均不推荐用于妊娠期妇女,因其在动物研究中均显示有生殖毒性。VKA 在妊娠早期会导致胎儿致畸,且VKA 可透过胎盘屏障,可能引起胎儿出血。UFH、LMWH 不会穿过胎盘,未发现 UFH、LMWH 具有胎儿毒性或致畸性,但可能会导致胎盘子宫壁交界区的出血。在接受磺达肝癸钠抗凝治疗的新生儿脐带血浆中发现抗 Xa 因子活性,目前磺达肝癸钠使用证据不够充分,建议孕妇避免使用。纳入一项系统评价,共计 2603 例孕妇,比较了依诺肝素、达肝素以及那屈肝素预防血栓的疗效与安全性,最终 VTE 发生率为0. 84%,孕妇出血率为 2%。相比 UFH、LMWH,出血事件发生率更低。对肝素类药物不耐受的患者,如肝素诱导的血小板减少症的患者,可选择磺达肝素钠。磺达肝素钠半衰期较长,因此需要在预产期 5 d前开始使用。孕妇由于孕期体重变化较大,给药时应当根据其体重调整药物剂量。
孕妇一旦开始分娩,应当立即停用 LMWH。考虑到 UFH 半衰期更短,便于逆转,有研究支持在 36~37周时将 LMWH 改为 UFH 进行 VTE 预防。
推荐意见 (1)对于妊娠期妇女,需要药物预防VTE 时,推荐首选预防剂量的 LMWH(1B)。(2) 建议在分娩时或剖宫产前 24h 停用 LMWH(2B)。(3)阴道分娩后 6~12 h、剖宫产术后 12~24 h 即可恢复抗凝治疗。有短暂产前或产时危险因素的妇女,建议接受产后血栓预防直到出院或产后两周(2C)。有持续危险因素的妇女(如肿瘤)建议接受产后 VTE 药物预防至少 6 周(2B)。
PICO 11:哺乳期妇女预防 VTE 抗凝药物的选用?
NOACs 通过乳汁分泌,可在乳汁中检测到相应的含量,因此禁用于哺乳期妇女。若必须使用应停止哺乳。磺达肝癸钠可泌入大鼠乳汁中,目前尚不知道磺达肝癸钠是否分泌入人乳中,在使用磺达肝癸钠期间不推荐哺乳。根据目前的研究结果,VKA、UFH 和 LMWH 在哺乳期使用对新生儿是安全的。
推荐意见 (1)推荐哺乳期患者使用 VKA、UFH、LMWH 进行 VTE 预防,不影响母乳喂养(1B)。(2)对于母乳喂养的妇女,不推荐使用直接凝血酶抑制剂和 Xa 因子抑制剂(1C);使用磺达肝癸钠期间不推荐哺乳(1C)。
PICO 12:儿童 VTE 防治抗凝药物的选用?
儿童 VTE 预防研究的人群包括先天性心脏病、肠外营养、中心静脉置管、急性淋巴细胞白血病和干细胞移植等,临床研究类型多样,样本量多为 100 例以下。一项随机对照试验纳入 500 例儿童 VTE 患者,中位随访 91 d,利伐沙班组 VTE 复发和出血事件发生率与对照组(肝素或转为 VKA)没有显著性差异,但利伐沙班组血栓完全消退的比例显著高于对照组(P<0. 05,OR =1. 70,95% CI:1. 11~2. 58)。目前利伐沙班在 EMA、日本已经获批儿童 VTE 治疗。其余推荐根据循证证据汇总如下。
推荐意见 (1)髋关节手术、骨盆和股骨截骨术、选择性脊柱手术、创伤后 VTE 的发生率较低,儿童不建议药物预防 VTE(2C)。(2)>13 岁儿童如预计>48 h 行动受限,应评估血栓和出血风险。低中危应确保饮水、早期运动、尽早移除中心静脉置管,考虑机械预防,如高危且无出血风险推荐药物预防(1B)。(3)对于急性淋巴细胞白血病患儿化疗,特别是使用 L-天冬酰胺酶期间,静脉血栓风险高,建议使用 LMWH预防(2C)。(4)心导管检查儿童,建议给予普通肝素或阿司匹林预防(2C)。(5)中短期中心静脉置管儿童,不建议常规预防血栓(2C)。(6)对于通过动静脉瘘进行血液透析的儿童患者,建议常规使用 VKA 或LMWH 预防血栓。对于通过中心静脉置管进行血液透析的儿童患者,建议常规使用 VKA 或 LMWH 血栓预防(2C)。(7)对于儿童 VTE 患者,推荐选择 VKA、肝素或利伐沙班进行单药治疗(1B)。
PICO 13:进食对口服抗凝药物的影响?
相关信息主要源于药品说明书与在线数据库,不提供证据等级与推荐强度。利伐沙班片剂 10 mg 的绝对生物利用度高(80%~100%),进食对 AUC 或无影响。但是对于 15 mg 或 20 mg 的利伐沙班片剂,空腹条件下服用吸收并不完全,与食物同服后,有较高的生物利用度,因此利伐沙班 15 mg 或 20 mg 应与食物同服。进食会使艾多沙班的生物利用度增加6%~22%。对于贝曲沙班,当喂食低脂(900 卡路里,20%脂肪)或高脂(900 卡路里,60% 脂肪)膳食时,与禁食状态相比,低脂饮食的 C max 和 AUC 分别平均减少了 70%和 61%,高脂饮食的 C max 和 AUC 分别减少了50%和 48%,因此服用贝曲沙班时,尽量避免与食物同服。其他 NOACs 与食物相互作用不明显,可与或不与食物同时服用。此外,当患者需要鼻饲时,粉碎后给药并不会改变阿哌沙班、利伐沙班和依度沙班生物利用度,打开达比加群胶囊后鼻饲给药,生物利用度大幅增加,增加出血风险。
对于华法林,多种食物会对其药效产生影响,其中能增强华法林药效的有: 大蒜、生姜、花椒、胡萝卜、木瓜、西柚、芒果、葡萄柚、酒精(如合并肝疾病)和鱼油等;能减弱华法林药效的有:含大量维生素 K 的食物(大多为绿色蔬菜及叶子如菠菜、带皮的黄瓜、木瓜、西芹、水芹、花菜、甘蓝等,动物肝)、绿茶、肠道营养剂、鳄梨、紫菜等藻类和黄豆及豆制品等。
推荐意见 (1)食物对 VKA 的抗凝作用影响较大,建议教育患者在 VKA 服药期间尽量保持饮食习惯稳定,尽量避免大量服用对抗凝作用影响较大的食物。对于饮食结构波动较大的患者,建议增加 INR 监测频率。(2)推荐服用 15 mg/20 mg 的利伐沙班时,与食物同服;服用贝曲沙班时,尽量避免与食物同服;其他 NOACs 和 10 mg 利伐沙班与食物相互作用不明显,可与或不与食物同时服用。
PICO 14:伴低蛋白血症患者 VTE 预防抗凝药物的选用?
低蛋白血症诊断标准:血清白蛋白小于 25 g或总蛋白小于 60 g。严重的低蛋白血症是造成血栓栓塞的重要因素之一。经检索,目前低蛋白血症患者的 VTE 预防的循证证据主要集中在肾病综合征(NS)的患者中,血栓栓塞事件是 NS 患者发病和死亡的一个可预防的因素,然而目前预防性抗凝并不普遍。
最终纳入 4 项原始研究。1 项 RCT 研究比较了LMWH在白蛋白<20 g·L-1 的患者中,LMWH 用于高血栓风险的成人 NS 患者相比给予 UFH 的对照组出血发生率更低,并且安全有效。另外两项为国内小样本 RCT 研究,口服利伐沙班与 VKA 预防肾病综合症低蛋白血症患者深静脉血栓、肺栓塞的疗效相当。但 VKA 的出血事件、药物调整次数均高于利伐沙班,并有停药改用其他药物的事件发生。另一项纳入 898 例患有原发性膜性肾病的患者的初始队列研究发现,对于低出血风险的患者,白蛋白水平<20g·L-1 的患者更容易从抗凝治疗中获益;但对于高出血风险的患者,无论血清白蛋白水平如何,患者均不大可能在抗凝治疗中获益。
综上可见,对于 NS 患者,短时间(1 个月)预防性抗凝,推荐首选 LMWH,剂量为 4000~5000 U·d-1 ;长期预防抗凝可选择利伐沙班或 VKA。若口服VKA,通过监测 INR 调整剂量,INR 控制在 2~3。选择利伐沙班,15 mg·d-1 。在低蛋白血症的患者中,当患者服用蛋白结合率高的药物时,药物在血浆中发挥作用的游离药物浓度会大大增高,从而可能引发不良事件。常用抗凝药物及其血浆白蛋白结合率:普通肝素(80%)、VKA(97%)、利伐沙班(95%)、阿哌沙班(87%)、艾多沙班(55%)、达比加群(35%)和贝曲沙班(60%)。低蛋白血症患者使用高蛋白结合率的抗凝药物,应密切监测患者凝血指标,必要时及时调整剂量。
推荐意见 (1)对于中低出血风险的肾病综合征患者,当血清白蛋白水平 < 20 g·L-1 时,建议短期治疗可首选 LMWH(2B)。序贯抗凝治疗可选择利伐沙班或 VKA(2B)。高出血风险患者避免使用抗凝药物。(2)低蛋白血症患者使用高蛋白结合率的抗凝药物,应密切监测患者凝血指标,必要时及时调整剂量(1C)。
PICO 15:行经皮冠状动脉介入治疗(PCI)患者术前是否需要停用抗凝药物?
纳入 4 项回顾性研究。结论较为一致,PCI围术期患者不需停用口服抗凝药、无肠外抗凝药物桥接的策略是安全的,但应在综合评估(血栓栓塞风险和出血风险)的基础上谨慎地个体化决策。使用桥接抗凝方案是穿刺部位出血的独立预测因素。
推荐意见 建议对于长期口服 VKA 及 NOACs 的患者,在 PCI 围术期不需间断抗凝治疗,且无需肠外抗凝药物进行桥接(2C)。
PICO 16:骨科大手术围手术期 VTE 预防抗凝药物的选用?
相关循证医学证据集中在人工全髋关节置换(total hip arthroplasty,THA)、人工全膝关节置换(total knee arthroplasty,TKA) 和髋部骨折手术(hip fractures surgery,HFS)患者,这 3 类患者是 VTE 发生极高危人群,当伴有其他危险因素时,VTE 发生风险更高。
常用 Caprini 血栓风险因素评估表进行评估。VTE的预防措施包括基本预防(如术后抬高患肢)、物理预防(如足底静脉泵、间歇充气加压装置及梯度压力弹力袜等)和抗凝药物预防。根据 Caprini 评分选择具体的预防措施,可选用的药物见表 5。

关于预防抗凝药物的疗程,Meta 分析和随机试验显示,术后 2 周以内发生 VTE 的风险最高,而手术2 周以后 VTE 发生率显著降低。部分研究显示,与安慰剂相比,长期预防降低了 VTE 发生率,且大出血事件并未增加,但小出血风险可能增加。不同研究中骨科术后长期预防的持续时间有所差异。
推荐意见 (1)对于接受 THA 或 TKA 的低出血风险患者,推荐给予药物预防。首选 LMWH 或 NO-ACs(1B);在 NOACs 中,优选利伐沙班或阿哌沙班(1B)。对于不能使用 LMWH 和 NOACs 的患者,推荐选择磺达肝癸钠、普通肝素和 VKA(1B)。(2)对于接受 HFS 的患者或推迟或不能行手术的髋部骨折患者,采用上述类似的药物选择方案。但由于 NOACs 在HFS 患者中的应用尚未经过评估,在其安全性和有效性得到证实之前,倾向于避免在该人群中使用这一药物(2C)。(3)对于 THA、TKA 或 HFS 患者,推荐抗凝药物预防至少持续 10~14 日,HFS 术后最长持续 35日(1A)。
PICO 17:行乳腺手术的患者围手术期 VTE 预防抗凝药物的的选用?
纳入 11 项研究,行乳腺手术患者被给予不同低分子肝素进行 VTE 预防。研究主要依据 Caprini评分来判断发生深静脉血栓的风险,并决定相应的处置策略。对于乳房切除术(伴或不伴有乳房重建)患者,基于 Caprini 评分评估血栓风险,从而调整 VTE 预防方案是必要的。
推荐意见 (1)对于中、高度 VTE 风险且没有高出血风险的患者,建议使用 LMWH 或低剂量普通肝素(2B)。(2) 对于有中、高度 VTE 风险且伴有高出血风险或出血后果严重的患者,应在患者出血风险 降 低 后,给 予 肝 素 类 药 物 进 行 血 栓 预 防(2B)。(3)对于中、高 VTE 风险的患者建议术前2~ 12 h 给予肝素类药物进行预防,用至术后3~7d,在可自主活动或出院后停止使用。肿瘤患者可用至术后 4 周(1C)。
PICO 18:行妇科手术(子宫、卵巢等)的患者围手术期间预防 VTE 抗凝药物的选用?
妇科手术 VTE 预防的原始研究数量较少,无法进行荟萃分析。妇科手术主要涉及盆腔,是 VTE 的高危因素。对于行妇科手术的患者,应根据 Caprini 评分评估患者 VTE 风险等级,推荐意见主要参考国内外指南。
推荐意见 (1)对中、高危 VTE 风险,无大出血风险的需行妇科手术的患者,推荐给予 LMWH 或低剂量的普通肝素进行预防,预防用药时间为术后 6~12 h 内开始使用(1B)。(2) 对极高危血栓风险、无大出血风险的需行妇科手术的患者,采取机械性与药物联合预防;术后大出血风险较高者,推荐采取机械性、药物序贯预防,先机械性预防(间歇充气加压装置为佳),待出血风险降低后改为机械性与药物联合预防(1B)。(3)对于非肿瘤妇科手术患者,预防用药疗程为 7~10 d;对于行妇科恶性肿瘤手术的患者,建议术后药物预防持续 4 周(2C)。
PICO 19:出血性卒中患者 VTE 预防抗凝药物的选用?
出血性卒中往往被列在抗凝药物说明书中的禁忌一栏中,使用时需要非常谨慎。实际上对于有血栓风险的出血性卒中患者,给予抗凝药物是十分必要的。目前,脑出血后接受抗凝治疗的患者比例为6. 3%~48%。
研究发现,若提示患者出血停止,对于出血性卒中症状发生在 1~4d 内,活动较少的患者,可应用小剂量 LMWH 或 UFH 皮下注射以预防静脉血栓形成。低质量的证据表明,对于需要卧床的脑出血患者,在脑出血发生后的 1~4 d 内给予低分子肝素预防深静脉血栓是安全的,且未发现 LMWH 与后期的血肿扩大和较差的预后存在相关性。而给予 UFH可能会引发急性颅内出血的后果,增加致残率。系统评价结果表明,出血性卒中患者中早期抗凝显著降低肺栓塞发生率,但 DVT 发生率、血肿扩大和死亡率无统计学差异。对于有血栓风险的出血性卒中患者,是否启动抗凝治应根据个体化原则,综合考虑多种因素,如有无可逆/可治疗的出血原因、多发颅内微出血点、严重的颅内出血、高龄、中断抗凝期间发生出血、未控制的高血压、标准或低剂量 NOAC 治疗时发生出血、酗酒以及 PCI 后需要双联抗血小板等。经多学科合作评估,如患者血栓风险高、颅内出血复发风险低,可在出血性卒中发生后 4~ 8 周。考虑启动抗凝治疗,在启动抗凝治疗前应进行头颅 CT 或 MRI等影像学检查。
推荐意见 对于脑出血发生后短期内无法活动的患者,经多学科综合评估,如患者血栓风险高、颅内出血复发风险低,可在出血性卒中发生后 4~8 周考虑启动抗凝治疗,可选择 LWMH,在启动抗凝治疗前应进行头颅 CT 或 MRI 等影像学检查(2B)。
PICO 20:缺血性卒中患者预防 VTE 抗凝药物的选用?
纳入 5 项随机对照研究荟萃分析发现:急性缺血性卒中患者,卒中发生后给予抗凝药物 14 d,相比于未使用抗凝药物,患者死亡率有下降趋势,但差异没有显著性(P>0. 05,OR =0. 74,95% CI:0. 52~1. 04)。而深静脉血栓发生率有所下降(P <0. 001,OR:0. 21,95% CI:0. 15 ~ 0. 29),可选择 LMWH 或阿加曲班。其他 NOACs 需要更多证据支持。
对于急性缺血性卒中患者应行头颅影像学检查,评估有无出血转化。如无出血转化,根据卒中严重程度考虑启动抗凝治疗的时机:如为短暂性脑缺血发作(TIA),可在缺血性卒中发生 1~3 d 后启动抗凝治疗;如为轻度卒中,可在缺血性卒中发生≥3 d 后启动抗凝治疗;如为中度卒中,可在缺血性卒中发生≥6~8 d 后启动抗凝治疗;如为重度卒中,可在缺血性卒中发生≥12~14 d 后启动抗凝治疗;如患者有出血转化,经治疗后临床改善或无临床恶化,头颅 CT 或 MRI证实出血转化明显缩小,可考虑在缺血性卒中发生≥3~28 d 后启动抗凝治疗。
推荐意见 (1)溶栓后的抗凝治疗尚无定论,不推荐无选择的早期进行抗凝治疗(1C)。(2) 对于VTE 高危患者,在谨慎评估风险、效益比后慎重选择,应在 24 h 后使用抗凝药物。推荐选择 LMWH 或阿加曲班,疗程14 d(2C)。(3)对于缺血性卒中且 VTE 高危患者,启动抗凝治疗的时机应根据有无出血转化及卒中严重程度决定(2B)。
PICO 21:创伤性脑损伤患者 VTE 预防抗凝药物的选用?
创伤性脑损伤(TBI)患者发生 VTE 的风险很大。头部损伤的简易损伤评分≥3 是创伤患者 VTE 的独立预测因素。无预防性治疗的 TBI 患者 VTE 发生率高达 54%,采用机械预防的 TBI 患者 VTE 发生率为25%。随着 TBI 严重程度的增加,VTE 风险增加。
纳入 4 项原始研究,均为回顾性队列研究。一项研究在颅内出血 24 h 后通过脑 CT 提示出血稳定给予依诺肝素或普通肝素,治疗组的 DVT 发生率显著降低,但 PE 发生率和出血量的增加没有统计学差异。
另一项研究是对实施药物预防 VTE 的回顾性研究,医生自行决定是否使用抗凝药物,结果 VTE 的发生率、住院时长比较差异均无统计学意义(P> 0. 05),但是死亡率明显较高。第 3 项研究随访了受伤 72 h以内和72 h 以后接受肝素治疗的患者,结果表明 VTE发生率无显著性差异,早期应用肝素患者未出现出血或病情恶化的不良事件。而一项多中心的回顾性研究发现,接受 LMWH 后有 14. 5% 的患者出血进展,4. 1%需要神经外科干预,延迟药物预防启动时机(48 h 后) 也没有降低出血率,研究结论:无法证明LMWH 对 TBI 的安全性。综上可见,对 TBI 患者预防与不预防 VTE 的研究结果不一致,提供的研究质量证据较低。
推荐意见 目前尚无高质量研究支持对重症 TBI患者进行 VTE 预防。如果 TBI 患者出现了 VTE,脑损伤稳定且评估抗凝治疗益处超过颅内出血风险,且无使用抗凝药物的相关禁忌,则建议可考虑使用抗凝药物,如 LMWH 或 UFH(2C)。
PICO 22:动脉瘤性蛛网膜下腔出血手术患者抗凝药物的选用?
动 脉 瘤 性 蛛 网 膜 下 腔 出 血 ( aneurysmal subarachnoid hemorrhage,aSAH)患者是 VTE 高风险人群,急性下肢深静脉血栓发生率为 1. 5%~24. 0%,肺栓塞发生率为 1. 2%~2. 0%。
该临床问题原始研究较少,多为亚组分析。纳入3 项原始研究。普通肝素能降低 DVT 的风险。LMWH 也可以降低 DVT 的风险,但同时会增加颅内出血风险。接受 LMWH 治疗的神经外科患者出血率会显著高于接受机械治疗的患者(P<0. 001),因此,处理动脉瘤前不建议使用药物预防。
由于 aSAH 患者 VTE 发生率较高,建议对所有患者在治疗动脉瘤破裂后的 24 h 内应始终进行间歇性气动加压治疗,并持续使用普通肝素,直到患者能活动为止。在动脉瘤夹闭或弹簧圈闭合后可以根据情况考虑使用 UFH 或 LMWH 预防。神经功能和生理状况稳定、缺乏血管痉挛的临床和(或)超声证据处于良好功能评级的 aSAH 患者,早期活动有助于减少VTE 的发生。
推荐意见 建议 aSAH 的患者,在动脉瘤外科或栓塞手术后 24h 内使用普通肝素预防 VTE,直至患者可下床活动(2C)。
PICO 23:颅内肿瘤患者围手术期 VTE 预防抗凝药物的选用?
纳入两项随机对照研究,一项为国内的 LMWH预防神经外科脑肿瘤术后 VTE 形成的 RCT,一共纳入 86 例患者,最终 LMWH 治疗组 VTE 发生率为4. 65%,显著低于对照组的 23. 26%,颅内血肿发生率无显著区别。另一项双盲随机对照研究,共纳入103 例、年龄均在 40 岁或以上的幕上肿瘤手术患者。
这些患者接受了小剂量的5000 U 肝素(55 例)或安慰剂(48 例)治疗,手术前 2 h 给药,直到肝素化或用药持续 7 d。研究结果表明,给予低剂量肝素预防 VTE未增加患者出血倾向。此外,还纳入 3 项回顾性的队列研究,分别针对脑膜瘤、胶质瘤的患者使用肝素或 LMWH 进行预防,均得到了类似的结果。
推荐意见 对于颅脑肿瘤患者,建议术前 2 h 给予低剂量的肝素或 LMWH,可 降 低 VTE 发 生 的风险(2C)。
PICO 24:腹部(非肿瘤)手术患者围手术期 VTE 预防抗凝药物的选用?
检索了肝胆手术、胰腺手术和脾切除等相关手术的 VTE 预防,原始研究较少,质量偏低,最终仅纳入 2项回顾性研究(分别为一项肝切除术与一项胰腺手术)。目前,肝切除术后 VTE 药物预防的特定方案及抗凝作用仍存在争议。对于肝手术的患者,术后一旦止血充分,应立即在所有肝手术患者中开始 VTE预防,是否存在出血可通过血液动力学稳定性、临床检查、血红蛋白水平和持续输血需求等指标来确定。
对于没有术后出血证据的住院患者,应继续进行 VTE预防抗凝,直至出院或完全恢复活动。胰腺手术的患者在术后 24 h 给予依诺肝素每天 4000 U 预防 VTE,所有预防的患者均未出现栓塞,且出血率较低。
推荐意见 (1)对于未发生严重出血并发症、高VTE 风险的(Caprini 评分≥5)普通外科手术或腹部手术患者,应接受 LMWH 或小剂量 UFH 的进行抗凝预防(1C)。(2)在中、高度 VTE 风险合并出血风险增加(如接受肝切除术)的外科患者中,当充分止血及术后出血风险降低时,在预期失血量最小的各种情况下进行术前抗凝预防血栓可能是合适的(1C)。(3)在肝手术后发现出血的,一旦止血充分,应立即在此类患者中给予 LMWH 或小剂量 UFH 进行预防,直至出院或完全活动恢复(2C)。(4)对于胰腺手术后的患者,建议术后采用间歇性气动压迫预防,同时在术后24 h 联合使用依诺肝素(4000 U·d-1 )预防,用药持续至患者可下地行走(2C)。
PICO 25:血液肿瘤患者预防 VTE 抗凝药物的选用?
血液肿瘤的患者 VTE 发生率约为 10%。多发性骨髓瘤(multiple myeloma,MM)VTE 发生率最高,尤其是联合使用了免疫抑制剂时。对于血液肿瘤患者,建议对住院卧床患者与门诊患者进行不同处置。
对于不卧床的血液肿瘤患者,可以使用 Khorana 风险评估模型评估 VTE 发生风险(表 6),总分≥3 分为高风险,总分为 1 或 2 为中风险,总分为 0 分为低风险。对 3 分及以上的患者给予抗凝药物预防是可以获益的。该模型已被国际指南推荐使用。对于住院的血液肿瘤患者,在纳入的回顾性研究中,患者VTE 发生的风险均较高。推荐进行预防性抗凝治疗,可选择肝素类药物进行预防。

免疫调节剂(IMiD)目前是 MM 的标准治疗手段。对于接受免疫抑制剂(沙利度胺/来那度胺/泊马度胺)的 MM 患者,VTE 的发生率显著升高。研究表明,对于接受免疫抑制剂的患者,强制进行 VTE 药物预防是必要的。一项前瞻性观察研究发现,接受低分子肝素预防的多发性骨髓瘤患者静脉血栓形成风险显著降低 87%。一项最新的阿哌沙班 2. 5 mg用于 MM 患者的一级预防的研究结果表明:给予低剂量阿哌沙班预防用药 6 个月,安全且耐受性良好。
患者的危险因素:(1)常规因素:肥胖(BMI>30kg·m-2 );既往 VTE;中心静脉导管或起搏器;罹患:心脏病、慢性肾病、糖尿病、急性感染、制动;手术:任何感觉缺失,创伤,应用促红细胞生成素,凝血障碍。(2)骨髓瘤药物治疗危险因素:免疫抑制剂:包括沙利度胺/来那度胺/泊马度胺联合:高剂量地塞米松(每月≥480 mg)或阿霉素;多药化疗。根据以上危险因素,若无危险因素或只有 1 项危险因素,可以使用阿司匹林 81~325 mg 进行预防;具有两个或以上相关危险因素的多发性骨髓瘤患者推荐用 LMWH (等量依诺肝素 40 mg·d-1 )或剂量调整的 VKA (INR2~3) 预防静脉血栓栓塞。
推荐意见 (1)对于住院的血液肿瘤患者,建议进行预防性抗凝治疗。可选择皮下注射 LMWH、磺达肝癸钠或普通肝素(2C)。(2)对于门诊血液肿瘤患者,根据 Khorana 风险模型评分,建议给予评分≥3 分的患者进行抗凝药物预防,可选择 LMWH 或者 VKA(2C)。(3)对于多发性骨髓瘤患者,建议根据患者的危险因素以及是否治疗用药情况给予阿司匹林、LMWH、VKA 或阿哌沙班进行预防(2B)。
PICO 26:服用抗凝药物导致出血事件时应如何处理?
首先应对出血的严重程度进行评估,大出血与非大出血事件的处理原则有所不同。
大出血:符合以下任何 1 项及以上,都属于大出血。①发生于关键部位的出血。②血流动力学不稳定。③血红蛋白下降≥2 g·dL-1 或需要输注浓缩红细胞≥2 U。
推荐意见(1)对于因抗凝药物引起的大出血,推荐立即停用抗凝药物。对于服用剂量较大、时间较短者推荐采用洗胃、活性炭治疗(1B)。(2)除给予患者内、外科的常规救治措施以外,若出现威胁生命或关键部位出血,推荐使用相应抗凝药物的拮抗剂(1A)。
非大出血:除大出血以外的所有出血。决策时需考虑以下问题:①抗凝是否超过治疗范围? ②抗凝是否在治疗范围内? ③是否即将进行侵入性操作? ④患者的潜在出血风险是否发生了变化(如增加新的药物,肝、肾功能急剧恶化等)? ⑤是否对出血部位和临床影响提供持续的诊断评估? ⑥患者的基线是否存在严重贫血,需输注浓缩红细胞≥1 U? ⑦患者是否存在相关医学并发症、虚弱或其他的医学问题(如心肌梗死或心肌缺血)?⑧是否存在关键部位缓慢出血而需要重复扫描(如早期扫描阴性的脑外伤导致的硬膜下血肿)?
非大出血患者大多数都需要停用(至少短期内)抗凝药物。是否停用取决于患者个体特点、患者和家人的意愿、出血性质和抗凝药物强度。
推荐意见 对于非大出血的患者,建议大部分患者均可停用(至少短期内)抗凝药物(2C)。如果确定患者不需要住院、手术或输血,并且已经止血,则可以继续使用抗凝药物(2C)。如果停用抗凝药物后出血仍无法控制,需使用相应的抗凝药物拮抗剂(2C)。
PICO 27:不同抗凝药物出血拮抗剂应该如何选择与使用?
PICO 27 -1 肝素类抗凝药物拮抗剂—鱼精蛋白的选择和使用鱼精蛋白是肝素的特异性拮抗剂,通过与肝素分子结合,解离肝素 - 抗凝血酶Ⅲ复合物,从而使肝素失去抗凝活性。鱼精蛋白只能部分中和 LMWH,且无法中和磺达肝癸钠。在有关鱼精蛋白拮抗普通肝素的系统评价和 meta 分析研究中,鱼精蛋白应用于颈动脉内膜切除术后拮抗肝素的抗凝活性,能够降低术后出血风险且不增加血栓事件。鱼精蛋白用于冠状动脉血管成形术后拮抗肝素抗凝活性,也能够安全有效地降低出血事件。此外,采用 Hepcon-HMS系统进行鱼精蛋白剂量滴定的方案也优于鱼精蛋白固定剂量方案,能够更好降低术后出血风险。鱼精蛋白与肝素的比例在 1∶1 以下的小剂量方案止血效果较好。应用 Hepcon - HMS 系统指导的鱼精蛋白/肝素剂量方案与固定剂量方案相比,鱼精蛋白剂量降低,术后出血量减少,且不增加血栓事件。
PICO 27 -2 维生素 K 抑制剂类抗凝药物拮抗剂—维生素 K 的选择和使用小剂量给予维生素 K(1 mg)皮下注射与静脉注射均难以快速有效纠正 INR 值,需要更高剂量才能够快速、完全逆转 VKA 的抗凝作用。对于门诊 INR>10的未出血患者,小剂量口服维生素 K(2 mg)同时停用VKA,能够安全有效地逆转 VKA 引起的凝血障碍。一项前瞻性研究发现:口服维生素 K 10mg 可安全、有效地部分逆转过量 VKA 引起的 INR 升高(5< INR <10)。对于服用 VKA 严重出血的患者,停药的同时给予肌注或静脉缓慢注射(静脉注射可能会不耐受)维生素 K 2. 5~10 mg,可逆转 VKA 过量,降低出血事件发生率。
PICO 27 -3 抗凝药物非特异性拮抗剂—凝血酶原复合物(PCC)的选择和使用凝血酶原复合物单独应用或联合维生素 K,能够逆转维生素 K 抑制剂类抗凝药物的抗凝作用以及相关性出血。一项系统评价研究结果显示:PCC 尤其是 4- 凝血酶原复合物能够逆转维生素 K抑制剂相关的 INR 升高,且优于新鲜血浆。目前,现有凝血酶原复合物拮抗抗凝药物的队列研究证据质量均较低。在纳入的研究中,PCC 根据初始 INR 值和体重进行个体化剂量调整(若 2≤INR <4,剂量为 25U·kg-1 ;若4≤INR<6,剂量为35 U·kg -1 ;若 INR>6,剂量为 50 U·kg-1 ,若患者体重大于 100 kg,按照100 kg 进行计算),联合不同剂量维生素 K 方案,能够有效快速逆转维生素 K 抑制剂类口服抗凝药物引起的出血,恢复 INR 值至正常水平。另一方面,PCC 联合维生素 K 与新鲜血浆联合维生素 K 相比,逆转维生素 K 抑制剂抗凝作用的效果更好,且降低出血风险。PCC 对于 NOACs(利伐沙班、阿哌沙班、艾多沙班、)抗凝活性同样具有逆转作用,两项入组人群特征基本一致的多中心、前瞻性、观察性研究显示,直接Xa 因子抑制剂相关出血使用 PCC 及特异性拮抗剂的止血效果和安全性均相似,但是达比加群效果不佳。
PICO 27 -4 达比加群特异性拮抗剂—依达赛珠单抗的选择和使用
依达赛珠单抗(idarucizumab)是一种人源单克隆抗体的片段,结构类似于凝血酶,但其与达比加群的结合能力是凝血酶的 350 倍,是达比加群特异性拮抗剂。常规推荐剂量为 5g。现有的系统评价和 Meta 分析研究显示:依达赛珠单抗是最优的逆转达比加群抗凝活性的拮抗剂。另一项系统评价研究显示,依达赛珠单抗可用于接受达比加群治疗出血或需要紧急手术患者的逆转治疗。
依达赛珠单抗能够快速、完全地逆转达比加群的抗凝活性。依达赛珠单抗 5 g 剂量能够快速、安全和持久地逆转达比加群的抗凝活性,用于控制接受达比加群治疗患者危及生命的出血以及需要紧急手术的患者。
利伐沙班和阿哌沙班的特异性拮抗剂 Andexxya,目前已经在美国和欧洲(有条件批准)获批上市。
推荐意见 见表 7。

PICO 28:使用肝素类抗凝药物出现肝素诱导的血小板减少症(HIT)时应该如何处理?
HIT 是在应用肝素类药物过程中出现的、由抗体介导的肝素不良反应,临床上以血小板计数降低为主要表现,可引发动静脉血栓形成,严重者甚至导致死亡。HIT 患者一经诊断或者高度怀疑应立即停用肝素,并接受非肝素类抗凝药物治疗,特别是肝素诱导的血小板减少症合并血栓形成(HITT)或存在继发血栓风险的患者。HIT 临床实际发生率很低,HIT 治疗多为小样本的随机前瞻研究、回顾性病例对照研究或个案报道。随着 NOACs 的问世及 HIT 诊断手段的发展,出现 NOACs 在 HIT 治疗中的相关研究报道。
HIT 治疗分为初始治疗(急性期治疗)和维持治疗(远期治疗)。(1)初始治疗(急性期治疗):首先停用肝素类抗凝药物,选用非肝素类抗凝药,主要为胃肠外给予比伐卢定、阿加曲班、或 NOACs,LMWH类不能作为替代治疗。在急性 HITT 患者中,建议在血小板计数未恢复到≥150 ×10 9 /L 前,不推荐使用 VKA。急性 HITT 发生时服用 VKA 的患者,立即停用 VKA,同时静脉注射维生素 K,并与非肝素抗凝剂同时使用。对于亚急性 HIT 患者,建议使用 NOACS(如达比加群、利伐沙班或阿哌沙班)进行治疗。(2)维持治疗(远期治疗):维持治疗多以 VKA 替代,个别情况下(如孕妇)可使用达肝素,慎用磺达肝癸钠。近年来也有相关报道探讨 NOACs 应用于维持治疗。对于需要 VTE 治疗或预防的远期 HIT 患者,建议使用非肝素抗凝剂(如阿哌沙班、达比加群、达肝素、艾多沙班、磺达肝癸钠、利伐沙班或 VKA),而不是 UFH 或LMWH。
推荐意见 (1)对于初期确诊急性 HIT 的患者,停用肝素类抗凝药物,推荐非肝素类抗凝药如比伐卢定、阿加曲班、或 NOACs(1C)。(2)对于合并有血栓的急性期 HIT 患者(HITT),血小板计数≥150 ×10 9 /L时,不推荐使用 VKA。若正在服用 VKA,需停用,同时静脉注射维生素 K 联用非肝素类抗凝药物(1C)。(3)对于需要维持治疗的 HIT 患者,推荐选择 VKA。个别情况下(如孕妇)可使用达肝素(2B)。
PICO 29:长期服用 VKA 患者 INR 值突然异常时如何进行剂量调整?
VKA 的 INR 值易受合并用药、饮食、用药依从性和机体状态(疾病、体重)等变化而波动,因此突发的INR 超出目标范围,应密切关注和分析引起波动的原因并加以控制。对于以前 INR 控制稳定的患者,单个稍微超范围的 INR 可能代表随机变化,调整 VKA 剂量可能没有必要,而且实际上可能会破坏 INR 的稳定性,导致控制不佳。该临床问题证据来源非原始研究,不提供证据等级与推荐强度。
推荐意见 (1)对于以前 INR 值稳定在目标范围内的患者,其单次的 INR 超出目标范围 < 0. 5 个 INR单位(低于或高于 INR 目标范围),应寻找 INR 波动的原因,包括依从性、药物食物之间的相互作用等因素,如找到相关因素,建议继续使用当前 VKA 剂量,纠正影响因素,并在 7~14 d 内继续当前剂量并重新测试 INR。(2)如 INR 值异常持续或超出范围值较大时,应调整 VKA 剂量(VKA 每周剂量增加或减少5% ~20%)。调整 VKA 每周剂量的最佳过程尚未确定。在进行剂量调整的 48 h 以后应密切复查 INR,并评估 VKA 稳定状态,确定是否需要进一步干预。保守剂量调整可防止矫枉过正和剂量失稳,更频繁的INR 监测可确保抗凝治疗的回归。发生原因不明的INR 波动时,立即增加或降低 VKA 剂量的依据不足。
PICO 30:VTE 患者在抗凝期间发生出血事件,后续是否重启抗凝治疗? 若需要如何选择抗凝药物?
首先应对患者进行出血风险评估:3 个月出血风险为低危的患者应当重启抗凝,重启抗凝预防血栓栓塞性疾病复发的好处将超过再次出血的风险。3 个月出血风险为高危的患者不应重启抗凝。对于出血风险中危的患者,目前尚无统一意见。对于大多数将恢复抗凝治疗的患者可以在出血消退后大约两周内恢复。
出血风险较低的 VTE 患者需要重新接受抗凝治疗。疗程分为长期抗凝和无限期抗凝,两者都涉及到最初 10 d 的初始抗凝:初始抗凝(最初 10 d):是指在诊断 VTE 后最初数日(最长达 10 d)进行的全身性抗凝治疗。可以选择 LMWH、磺达肝癸钠、利伐沙班或阿哌沙班,或使用 UFH。VKA 不能单独作为 VTE 患者的初始抗凝药物,因为已形成的维生素 K 依赖性凝血因子需要一定时间才能被消耗。(2)长期抗凝(10日至至少 3 个月):指在最初数日抗凝后继续给予一段时间的抗凝,通常为 3~6 个月,部分情况下最长可达 12 个月(如有持续但可逆的危险因素)。
推荐意见 (1)出血风险较低的 VTE 患者重新开始短期抗凝治疗时,可选择 UFH、LMWH、磺达肝癸钠或 NOACs(2B)。不推荐使用 VKA(1B)。抗凝时间最短为 3 个月。(2)若患者无法选择凝血因子Ⅹa抑制剂或直接凝血酶抑制剂,或者有肾功能异常(肌酐清除率 <30 mL·min-1 ),VKA 是替代选择(2D)。
指南制定成员:
执笔人:王乔宇(首都医科大学附属北京天坛医院)、王晓岩(首都医科大学附属北京天坛医院)、武明芬(首都医科大学附属北京天坛医院)、柳鑫(首都医科大学附属北京天坛医院)、陈耀龙(兰州大学循证医学中心)和赵志刚(首都医科大学附属北京天坛医院)。
指南指导组:赵志刚(首都医科大学附属北京天坛医院)、张相林(中日友好医院)、郑英丽(中国医学科学院阜外医院)、朱珠(北京协和医院)、宋海波(中国毒理学会临床毒理专业委员会)、缪丽艳(苏州大学附属第一医院)、林厚文(上海交通大学医学院附属仁济医院)、卢晓阳(浙江大学医学院附属第一医院)、张冰(北京中医药大学)、翟所迪(北京大学第三医院)和张玉(华中科技大学同济医学院附属协和医院)。
指南专家组(按拼音顺序):蔡卫新(首都医科大学附属北京天坛医院)、曹玮(云南省第一人民医院)、陈丽娟(天津市胸科医院)、戴海斌(浙江大学医学院附属第二医院)、董占军(河北省人民医院)、封卫毅(西安交通大学第一附属医院)、付秀娟(吉林大学第二医院)、高申(海军军医大学第一附属医院)、葛卫红(南京大学医学院附属鼓楼医院)、郭瑞臣(山东大学齐鲁医院临床药理研究所)、郭伟(首都医科大学附属北京天坛医院)、侯锐刚(山西医科大学第二医院)、胡欣(北京医院)、黄品芳(福建医科大学附属第一医院)、黄欣(山东省千佛山医院药学部)、赖伟华(广东省人民医院)、李焕德(中南大学湘雅二医院)、李朋梅(中日友好医院)、李文歌(中日友好医院)、刘宝戈(首都医科大学附属北京天坛医院)、刘皋林(上海交通大学附属第一人民医院)、刘焕龙(河北医科大学第二医院)、龙恩武(四川省人民医院)、吕迁洲(复旦大学附属中山医院)、矛益民(上海交通大学医学院附属仁济医院)、邱峰(重庆医科大学附属第一医院)、石广志(首都医科大学附属北京天坛医院)、宋燕青(吉林大学第一医院)、隋忠国(青岛大学附属医院)、孙秀颖(天津市人民医院)、王伽伯(首都医科大学中医药学院)、王建华(新疆医科大学第一附属医院)、王硕(首都医科大学附属北京地坛医院)、王晓岩(首都医科大学附属北京天坛医院)、文爱东(空军军医大学西京医院)、吴玉波(哈尔滨医科大学附属第四医院)、谢娟(贵州省人民医院)、徐东(首都医科大学附属北京天坛医院)、徐萍(天津第五中心医院)、于荣(山西省心血管病医院)、张冰(北京中医药大学)、张洪义(首都医科大学附属北京天坛医院)、张峻(昆明医科大学第一附属医院)、张倩(南京市第一医院)、赵春景(重庆医科大学附属第二医院)、赵性泉(首都医科附属北京大学天坛医院)和肈丽梅(中国医科大学附属盛京医院)。
循证秘书组(按拼音顺序):王红梅、幸晓琼、杨佳丹 (重庆医科大学附属第一医院);杜青青、赵春景(重庆医科大学附属第二医院);边原、韩丽珠、尹琪楠(电子科技大学附属医院);王航 (福建医科大学附属第一医院);李晓宇、陈灿(复旦大学附属中山医院);曾英彤、周婧(广东省人民医院);李黎、谢娟、张家兴(贵州省人民医院);刘宣彤、孙向菊、吴禹蒙(哈尔滨医科大学附属第四医院);王卓、钱皎、曹爱霖(海军军医大学第一附属医院);赵宜乐(河北省儿童医院);田冬冬、赵越(河北省人民医院);杨珍珍(河北医科大学第二医院);高立娜、刘雅竹、王司允(吉林大学第二医院);李艳娇、王鑫璐(吉林大学第一医院);张峻 、柳汝明(昆明医科大学第一附属医院);徐航、王宝彦(南京大学医学院附属鼓楼医院);张斌、纪洪艳、张传洲(青岛大学附属医院);杨依磊(山东第一医科大学第一附属医院);梁璐、王娟、闫云燕(山西省心血管病医院);王思扬、张瑞琴(山西医科大学第二医院);顾智淳(上海交通大学医学院附属仁济医院);凌曦、李雁铭、柳鑫、李茜茜、王雅君、王乔宇、叶佳丹(首都医科大学附属北京天坛医院);谢诚、赵瑞(苏州大学附属第一医院);谭晓旭、王舒(天津市第五中心医院);赵振营(天津市人民医院);胡占嵩、屠莹、张瑶(天津市胸科医院);郑巧伟(西安交通大学第一附属医院);蒲文、向云霞(新疆医科大学第一附属医院);黄帮华、闵秋霞(云南省第一人民医院);杨艳艳(浙江大学附属第一医院);徐慧敏(浙江大学医学院附属第二医院);丁征、于欢(中国医学科学院阜外医院)和赵莉(中日友好医院)。
指南外审组(按拼音顺序):安卓玲(首都医科大学附属北京朝阳医院)、卞晓岚(上海交通大学医学院附属瑞金医院)、苍爱军(辽宁省人民医院)、陈霞(南通市第一人民医院)、杜小莉(北京协和医院)、范国荣(上海市第一人民医院)、封宇飞(北京大学人民医院)、韩婧(贵州省人民医院)、何文(武汉人民大学)、胡锦芳(南昌大学第一附属医院)、菅凌燕(中国医科大学盛京医院)、姜德春(首都医科大学附属北京世纪坛医院)、金鹏飞(北京医院)、李贵茹(大连医科大学附属第二医院)、李静(青岛大学附属医院)、李雅秋(辽宁中医药大学附属医院)、刘建龙(北京积水潭医院)、刘韶(中南大学湘雅医院)、刘滔滔(广西医科大学第一附属医院)、刘烨(南昌大学第二附属医院)、吕永宁(华中科技大学同济医学院附属协和医院)、毛乾泰(北京清华长庚医院)、米玉红(首都医科大学附属北京安贞医院)、倪如炀(首都医科大学附属北京同仁医院)、沈爱宗(中国科学技术大学附属第一医院)、沈素(首都医科大学附属北京友谊医院)、史振宇(复旦大学附属中山医院)、束雅春(江苏省中医院)、魏理(广州医科大学附属第一医院)、吴晖(昆明医科大学第一附属医院)、伍俊研(中山大学孙逸仙纪念医院)、闫勇(首都医科大学附属北京世纪坛医院)、杨媛华(首都医科大学附属北京朝阳医院)、战寒秋(首都医科大学附属北京地坛医院)、张波(哈尔滨医科大学附属第二医院)、张登丽(江苏省人民医院)、张健(上海交通大学医学院附属新华医院)、张晓坚(郑州大学第一附属医院)、张亚明(盐城市第一人民医院)、张艳华(北京大学肿瘤医院)、张吟(福建医科大学附属第二医院)、赵荣生(北京大学第三医院)、赵渝(重庆医科大学附属第一医院)、甄健存(北京积水潭医院)和周晨霞(常熟市第二人民医院)。
参考文献:略
文章来源:中国临床药理学杂志第37卷第21期2021 年 11 月(总第 347 期)
医疗纠纷律师、医疗事故律师、安徽医疗纠纷律师、合肥医疗纠纷律师、安徽医疗事故律师、合肥医疗事故律师、医药健康律师、安徽医疗律师、合肥医疗律师、陈俊福律师


