中国抗癌协会肿瘤临床化疗专业委员会,中国抗癌协会肿瘤支持治疗专业委员会
恶心、呕吐是肿瘤药物治疗的常见不良反应。在我国,恶心、呕吐的预防和治疗以5-羟色胺(5-hydroxytryptamine,5-HT)3受体拮抗剂联合地塞米松作为主流方案,但30%的恶心、呕吐仍未获得满意控制,恶心、呕吐依然是困扰和影响患者生活质量的重要因素。肿瘤药物治疗相关恶心、呕吐显著影响患者的生活质量,降低患者抗肿瘤治疗的依从性,从而影响疗效。另外,严重的恶心、呕吐还可能导致脱水、电解质紊乱、自理能力下降、功能性活动受限、营养缺乏、焦虑、体力状况评分降低、伤口裂开、食管黏膜撕裂、治疗耐受性降低等严重后果。因此,结合该领域国内外最新研究进展,制定适用于我国现状的共识意见以指导临床治疗,具有非常重要的现实意义。
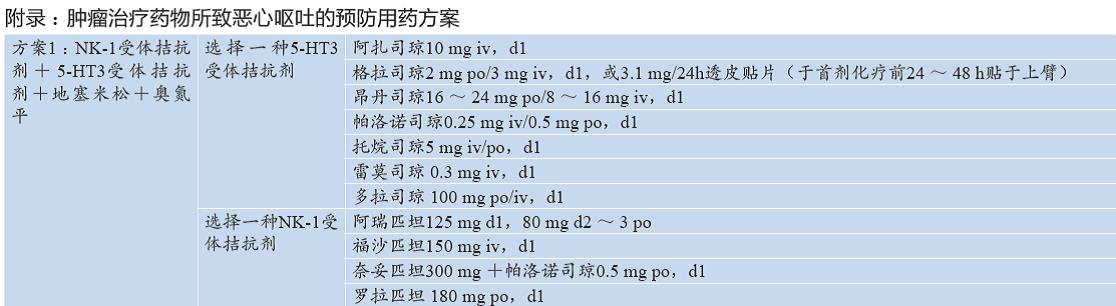
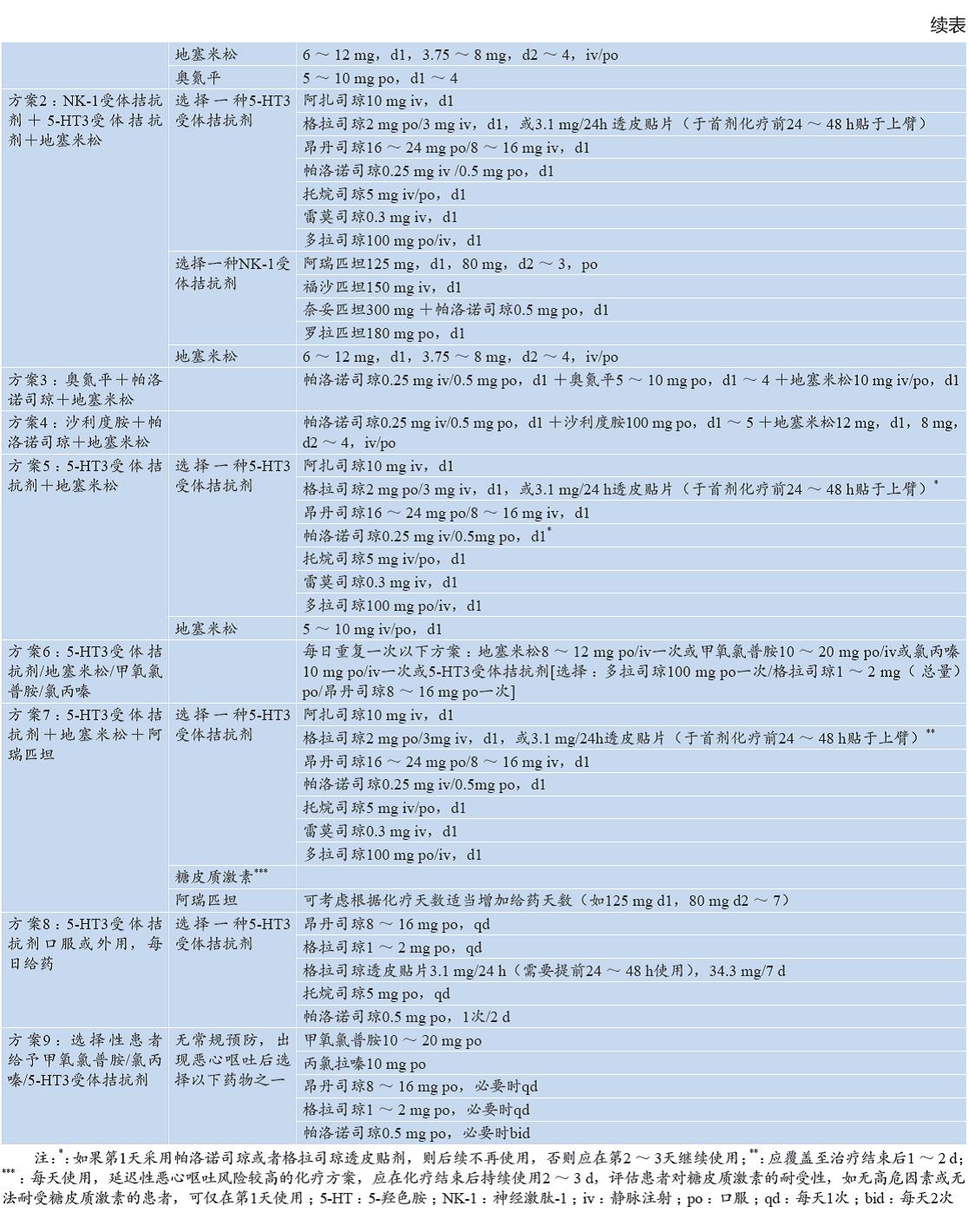
近年来,尽管在肿瘤药物治疗相关恶心呕吐的机制研究和新药研发方面取得了长足进展,但仍然存在诸多尚未解决的问题,如暴发性呕吐和难治性呕吐的治疗、恶心的机制及其治疗等。规范恶心、呕吐风险评估和预防处理,能够提高恶性肿瘤患者的治疗依从性和耐受性,改善生活质量,从而有望延长其生存时间。中国抗癌协会肿瘤临床化疗专业委员会和肿瘤支持治疗专业委员会组织国内肿瘤内科、放疗、妇科、护理、流行病学等领域的权威专家共同制定了本共识。本共识基于国内外最新研究进展并结合国内现状,对抗肿瘤药物治疗所致恶心呕吐的病理生理、分类分级、影响因素、预防和治疗原则进行阐述,并给予恶心呕吐预防和处理用药推荐(表1),期待为广大医务工作者的临床实践提供指引。本共识适用于接受抗肿瘤药物治疗的成年患者。

1 恶心呕吐的病理生理
呕吐是一个由大脑控制的多步骤反射过程。化疗所致呕吐的受体分布在延脑极后区,在肠嗜铬细胞附近的迷走神经末端也发现了这些受体。传入神经将信号传到脑干,进行呕吐反射处理,再将传出信号传递到不同的器官和组织,诱导呕吐。目前研究发现,抗肿瘤药物可以通过外周途径和中枢途径2条通路引起呕吐反射。外周途径一般在给予抗肿瘤药物24 h之内发生呕吐,通常表现为急性呕吐(0~24 h)。抗肿瘤药物诱导肠嗜铬细胞释放血清素,激活迷走神经的5-HT3受体,继而将信号传递到大脑。中枢途径主要位于大脑,一般在应用抗肿瘤药物24 h之后发生呕吐,通常表现为药物诱导的延迟性呕吐(25~120 h)。P物质是中枢神经系统中激活神经激肽-1(neurokinin-1,NK-1)的主要神经递质,与延迟性呕吐相关。5-HT3受体与NK-1受体相互交联,当一个受体被配体激活时,另一个受体也会被激活,但其中机制尚不完全清楚。目前使用的预防呕吐的药物包括多巴胺受体拮抗剂、5-HT3受体拮抗剂、NK-1受体拮抗剂。通常每种预防性药物主要阻断某一类受体,只有奥氮平能够作用于呕吐通路的多个受体。目前尚未发现诱发呕吐反应的共同通路,因此尚无一种药物能够对不同类型的恶心呕吐实现完全阻断。随着有效止吐药物的应用,接受致吐性抗肿瘤药物治疗患者的恶心发生率已高于呕吐。恶心和呕吐在发生机制上相互关联,但不尽相同。总体而言,年轻患者更易发生恶心;接受乳腺癌治疗的年轻女性较其他人群更易出现恶心;延迟性恶心较急性恶心更为常见,且程度更重,治疗更为困难(图1)。

2 抗肿瘤药物治疗相关恶心呕吐的分类
抗肿瘤药物治疗包括细胞毒药物化疗(以下简称化疗)、靶向治疗和免疫治疗,由于化疗导致的恶心呕吐(chemotherapy-induced nausea and/or vomiting,CINV)最为严重,故研究最为深入并且疗效确切,其他两种药物所致恶心呕吐均参考CINV的原则处理。CINV根据其发生时间和治疗效果可以分为急性、延迟性、预期性、暴发性和难治性。
急性CINV在化疗后数分钟至数小时内发生,常在24 h内缓解。急性CINV的高峰通常持续5~6 h。发生急性CINV患者的相关危险因素包括年龄<50岁、女性、低酒精摄入、情绪障碍等。其他影响急性CINV的因素包括既往治疗的恶心呕吐史、实施化疗的场所、致吐药物的剂量以及止吐药物的使用。
延迟性CINV发生在化疗24 h后,常发生于接受顺铂、环磷酰胺和蒽环类药物治疗的患者。例如,顺铂所致呕吐常在化疗后48~72 h达到高峰,可持续6~7 d。
预期性CINV发生于曾接受化疗的患者,在下一次化疗前即出现恶心呕吐,其发生常与既往化疗不愉快的体验相关。预期性CINV的发生率为18%~57%,其中恶心比呕吐更为常见。
暴发性CINV是指在预防性处理之后仍然出现的呕吐,并且需要给予止吐药物“解救治疗”的恶心呕吐反应。
难治性CINV是指在既往的化疗周期中使用预防性和/或解救性止吐治疗失败,而在后续化疗周期中仍然出现的呕吐。
3 化疗药物的致吐性分级
化疗药物诱导的呕吐反应的发生率主要与所使用化疗药物的致吐性相关。目前已有多种针对化疗药物致吐性的分级系统,临床普遍采用的是4分级法,该分级将化疗药物按照未进行预防处理时发生急性呕吐的风险比率分为高度、中度、低度和轻微4个致吐风险等级,分别对应的急性呕吐发生率为>90%、30%~90%、10%~30%和<10%。表2列举了常见化疗药物和组合的致吐风险级别。此外,化疗药物的联合使用和多疗程化疗均有可能增加恶心呕吐的发生风险。
抗肿瘤药物治疗相关恶心呕吐的发生率和严重程度受多种因素影响,包括:使用的治疗药物,药物的使用剂量,给药方式,放疗的靶区(如全身、上腹部)和患者的个体差异(如年龄、性别、既往治疗情况、饮酒史、合并用药情况、肿瘤侵犯部位、体能状态等)。

4 止吐药物的分类和机制
目前临床上常用的止吐药物根据其作用机制大致分为5-HT3受体拮抗剂、NK-1受体拮抗剂、糖皮质激素、非典型抗精神病药物、苯二氮䓬类药物、吩噻嗪类药物、其他类型的止吐药物等(表3)。

5 抗肿瘤药物治疗相关恶心呕吐的治疗原则
5.1风险评估 除化疗药物致吐等级不同外,还有多种因素会增加恶心呕吐发生风险。主要包括化疗相关因素(大剂量化疗药物,多种化疗药物联用,化疗药物静脉滴注速度快,接受多个周期化疗)和患者自身因素(女性、有晕动症或孕吐史、50岁以下、饮酒史、焦虑症、既往有化疗引起恶心呕吐史)。病史评估包括患者是否使用阿片类药物、存在不完全性或完全性肠梗阻、前庭功能障碍、肿瘤脑转移、电解质紊乱、尿毒症、肝功能异常等。
5.2 预防为主,注重全程与个体化管理 止吐治疗应先于抗肿瘤治疗,根据拟行抗肿瘤治疗方案的致吐风险、患者自身的高危因素、既往发生恶心呕吐的严重程度,制订个体化的防治方案。在末剂量给药治疗后,接受高度和中度致吐风险药物治疗的患者,恶心呕吐发生风险仍然将持续2~3 d,因此在整个风险期,均需对呕吐予以防护。同时,止吐方案的制订还应充分考虑同时使用的非抗肿瘤治疗导致恶心呕吐的风险(如患者合并使用阿片类镇痛药等)。在设计止吐方案时要考虑到实际问题,如处理时的背景( 住院患者或门诊患者)、首选给药途径( 肠外、口服或透皮)、5-HT3受体拮抗剂作用持续时间和给药间隔时间、患者对每日给予止吐药物(如糖皮质激素)的耐受性、依从性、顺应性问题和个体的风险因素(图2)。
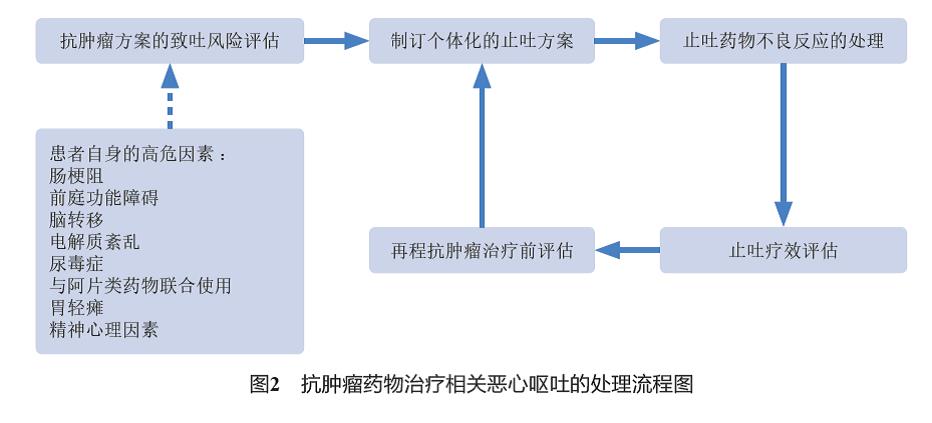
5.3 止吐药物的选择 根据抗肿瘤药物治疗的致吐风险、既往使用止吐药物的反应、恶心呕吐的性质、患者个体因素以及是单药还是联合应用进行药物的选择。
5.4 生活方式管理 良好的生活方式也能缓解恶心、呕吐,例如少食多餐,选择易消化、合胃口的食物,控制食量,避免食用辛辣刺激性食物,不吃冰冷或过热食物等。
5.5 注重再评估 在进行下一周期治疗前,重新评估并调整治疗方案,如出现暴发性呕吐则应考虑加强止吐治疗,如加用NK-1受体拮抗剂或奥氮平、换用不同药代动力学/药效学特征的NK-1受体拮抗剂、添加其他止吐药物、调整5-HT3受体拮抗剂的剂量( 强度或频率)、加用一种抗焦虑药物、考虑抑酸治疗(H2受体拮抗剂或质子泵抑制剂)等。如果化疗目标是非治愈性的,处理难治性呕吐时可考虑调整治疗方案。
6 肿瘤药物治疗所致恶心呕吐的预防
6.1 高致吐性方案所致恶心呕吐的预防 推荐在化疗前采用三药联合方案,首选5-HT3受体拮抗剂、地塞米松和NK-1受体拮抗剂的联用方案(1类证据)。在中国人群中开展的研究显示,沙利度胺联合帕洛诺司琼和地塞米松可以预防初治化疗患者的延迟性恶心呕吐,在减轻厌食方面也有优势(1类证据),是一种较为经济实用的三联方案。奥氮平作为精神类药物,具有嗜睡、镇静等不良反应,但可明显缓解肿瘤患者的焦虑和抑郁。本共识推荐对嗜睡、镇静等发生风险小,同时既往使用标准三联方案仍出现暴发性或难治性呕吐的患者,可考虑在三联方案基础上加用奥氮平,剂量为每日5 mg(1类证据)。在使用NK-1受体拮抗剂时,应注意减少地塞米松等激素用量,并注意与其他药物相互作用带来的药物代谢变化和相关影响。
6.2 中致吐性方案所致恶心呕吐的预防 推荐采用5-HT3受体拮抗剂联合地塞米松的标准二联方案(1类证据),对于有焦虑或抑郁倾向的患者,可考虑在此方案基础上加用奥氮平(1类证据)。对于伴有其他风险因素或既往使用“皮质类固醇+ 5-HT3受体拮抗剂”治疗失败的患者,应使用地塞米松+5-HT3受体拮抗剂+ NK-1受体拮抗剂联合方案(1类证据)。
6.3 低致吐性方案所致恶心呕吐的预防 建议使用单一止吐药物,推荐5-HT3受体拮抗剂、地塞米松、多巴胺受体拮抗剂(如甲氧氯普胺)或氯丙嗪预防呕吐(依据推荐强度排序,均为2A类证据)。
6.4 轻微致吐性方案所致恶心呕吐的预防 对于无恶心呕吐史的患者,不必在化疗前常规给予止吐药物(2A类证据)。如果患者发生呕吐,后续治疗前参照低致吐性方案所致恶心呕吐的预防进行处理(2A类证据)。
6.5 多日化疗所致恶心呕吐的预防
6.5.1 接受多日化疗的患者存在急性和延迟性恶心呕吐的双重风险,致吐潜能因个体所使用的化疗药物和使用顺序不同而异,因此难以对每天的止吐方案作出特定的推荐。
6.5.2 5-HT3受体拮抗剂联合地塞米松是预防多日化疗所致恶心呕吐的标准治疗,通常主张在化疗全程使用5-HT3受体拮抗剂,地塞米松应连续使用至化疗结束后2~3 d(2A类证据)。
6.5.3 对于高致吐性或延迟性恶心呕吐高风险的多日化疗方案( 如含顺铂的多日方案),可以考虑加入NK-1受体拮抗剂,NK-1受体拮抗剂的使用最多可延续至化疗第7天(2A类证据)。
6.5.4 复方奈妥匹坦/帕洛诺司琼胶囊兼具NK-1受体拮抗剂和5-HT3受体拮抗剂的作用机制,且使用方便,在多日化疗高致吐方案中可考虑使用(2A类证据)。格拉司琼透皮贴剂在疗效、不良反应和安全性方面与格拉司琼的其他制剂无差异,但可减少血药浓度波动,可平稳控制恶心呕吐达7 d,可作为多日化疗所致恶心呕吐的5-HT3受体拮抗剂之一(2A类证据)。
6.6 口服药物致恶心呕吐的预防
6.6.1 对中-高致吐风险方案,5-HT3受体拮抗剂可持续每日给药,推荐使用口服或外用剂型以增加患者给药的便利性和舒适性(2A类证据)。
6.6.2 对低-轻微致吐风险方案不做常规预防,仅在必要时给予5-HT3受体拮抗剂、甲氧氯普胺或氯丙嗪中的一种(均为2A类证据)。
抗肿瘤药物所致恶心呕吐的预防治疗方案见图3。

6.7 预防失败后止吐方案的调整 以下方案均可作为挽救方案的选择:若预防方案未包含NK-1受体拮抗剂,可考虑增加该药;从含NK-1受体拮抗剂的三联方案转变为含奥氮平的三联方案,或从含奥氮平的三联方案转变为含NK-1受体拮抗剂的三联方案,或含沙利度胺的三联方案;NK-1受体拮抗剂联合奥氮平四联方案;在方案中增加其他作用机制的药物( 如多巴胺受体拮抗剂或氟哌啶醇);调整5-HT3受体拮抗剂的给药剂量或给药频率;更换5-HT3受体拮抗剂的种类;增加抗焦虑药物;对于接受非根治性化疗的患者,如在调整止吐药物后仍然不能耐受或不愿意继续原方案,可考虑更换其他致吐风险更小的化疗方案;增加抑酸剂(H2受体拮抗剂或质子泵抑制剂)。
6.8 预期性恶心呕吐的治疗 预期性恶心呕吐是在给予化疗药物之前发生的恶心和呕吐。目前普遍认为它是一种经典的条件反射模型,受环境影响。最有效的方法是在每周期化疗时给予最佳止吐治疗,防止呕吐的发生。另外,避免接触刺激性、异味或臭味气体可有助于预期性恶心呕吐的治疗。一旦发生预期性恶心呕吐,推荐采取心理干预疗法,家属应营造温馨环境,分散患者注意力,使患者心情放松;也可以采用瑜伽、渐进性肌肉放松、催眠疗法、生物反馈疗法和系统性脱敏治疗等行为疗法。中医针灸对预期性恶心呕吐也有一定的作用。推荐抗焦虑药如劳拉西泮或苯二氮䓬类药物与止吐治疗联合(图4)。
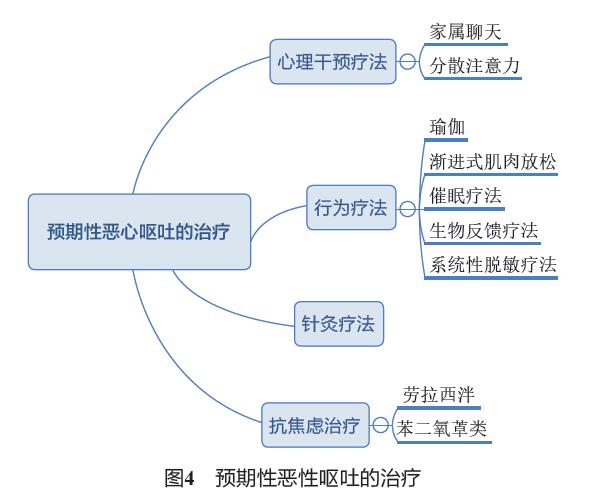
6.9 暴发性/难治性恶心呕吐的治疗 化疗过程中尽管给予了标准的预防性止吐处理,部分患者仍然会发生暴发性恶心呕吐。对此类患者,如果之前预防止吐方案中未使用奥氮平,推荐加用该药解救止吐。一项随机对照Ⅲ期临床研究对比了奥氮平与甲氧氯普胺在暴发性呕吐治疗中的作用,结果显示奥氮平与甲氧氯普胺相比,无恶心发生率分别为68%和23%,无呕吐发生率分别为70%和31%。若患者之前使用了奥氮平作为预防性止吐治疗,推荐采用预防止吐中未使用过的不同作用机制的止吐药物,如NK-1受体拮抗剂或氟哌啶醇、甲氧氯普胺、东莨菪碱透皮贴、类固醇激素、劳拉西泮和屈大麻酚等。在给药方式上,若患者呕吐非常明显,建议采用静脉给药、肌内注射、皮下给药、纳肛、贴剂等。
7 止吐药物不良反应及其处理
7.1 便秘 便秘是5-HT3受体拮抗剂最常见的不良反应,发生率为1%~ 11%,应用NK-1受体拮抗剂的患者也时有发生。止吐药物导致胃肠道分泌和蠕动功能受损是导致便秘最常见的原因,化疗药物如长春碱类等干扰胃肠功能,其他如大脑皮质功能受损、意识障碍和自主神经功能紊乱等均可引起便秘。可通过多饮水、多吃蔬菜水果和富含纤维素的食物软化粪便;鼓励患者适度活动,促进胃肠蠕动。可适当服用预防便秘的药物如乳果糖、麻仁丸、番泻叶等,便秘时可使用开塞露或肥皂条塞肛,必要时温盐水灌肠,但后者对颅内压增高患者要慎用。
7.2 头痛 轻微头痛是5-HT3受体拮抗剂和NK-1受体拮抗剂的常见不良反应,发生率为2%~10%。可予以热敷、按摩太阳穴等,必要时给予解热镇痛药,重症者可使用麦角胺咖啡因。
7.3 腹胀腹痛 腹胀腹痛是应用止吐药物的不良反应之一(发生率≥2%)。轻度腹胀不需特殊处理。明显腹痛腹胀者可行保守治疗,禁食、胃肠减压、肛管排气和应用解痉剂。腹胀严重导致肠麻痹者,可应用全肠外营养,使用生长抑素减少消化液的分泌和丢失,也可进行高压氧治疗,置换肠腔内氮气以减轻症状。
7.4 锥体外系症状 主要见于吩噻嗪类和多巴胺受体拮抗剂( 如甲氧氯普胺),发生率约为1%。应注意避免奥氮平、吩噻嗪类、甲氧氯普胺或氟哌啶醇同时应用导致多巴胺受体过度阻断,增加锥体外系症状的发生风险。锥体外系不良反应主要有4种类型:①急性肌张力障碍;②静坐不宁腿综合征;③Parkinson综合征;④迟发性运动障碍。发生后应立即停药。对于急性肌张力障碍者,可予以苯海拉明治疗。如对苯海拉明过敏,可使用抗胆碱能药物如苯托品、东莨菪碱、山莨菪碱、阿托品或苯二氮䓬类药物如地西泮。
7.5 心血管系统症状 发生率为0.1%~1%。主要表现为心律失常,如期前收缩、房室传导阻滞、QT间期延长、低血压和晕厥等。QT间期延长较为罕见( 发生率<0.1%),但是一个需要特别关注的5-HT3受体拮抗剂毒性问题。研究表明,大剂量的昂丹司琼可能引起QT间期延长,因此静脉注射昂丹司琼的单次最大剂量不应超过16 mg。
多拉司琼注射剂引起致命性恶性心律失常(尖端扭转型室性心动过速)的个案亦有报道,多拉司琼还可导致剂量依赖型QT、PR和QRS间期延长。当发生心电图异常时应立即停用相关药物,动态监测心电图变化,QT间期延长通常6~8 h恢复至基线,但有个别患者可持续24 h甚至更长时间。可予补液促进药物排泄,补钾、补镁。如果心率慢,可用异丙肾上腺素提高心率或临时起搏。总体而言,第一代5-HT3受体拮抗剂所致心律失常的死亡风险无统计学意义,透皮贴片剂型可以在一定程度上降低药物对QT间期的影响。第二代5-HT3受体拮抗剂的不良反应发生率低于第一代药物。
鉴于上述原因,专家组推荐:先天性长QT间期综合征、其他潜在的心脏疾病(如充血性心力衰竭、心动过缓)和电解质异常(如低钾血症、低镁血症)患者心律失常发生风险较高,在已经使用其他可能延长QT间期的药物(如精神类药物奥氮平、氟哌啶醇)时,已经或可能发展为心脏传导间期尤其是QT间期延长时,应慎用5-HT3受体拮抗剂,并定期进行心电图检查,密切监测QT间期变化情况。
7.6 过度镇静 奥氮平引起的过度镇静作用通常表现在用药第2天,发生率≥10%,可考虑减少给药剂量,该症状随着用药时间延长会逐步改善。此外,吩噻嗪类、苯二氮䓬类和氟哌啶醇可抑制中枢神经系统功能,导致过度镇静。联合用药时,应充分评估过度镇静的发生风险。有摔倒风险(如老年、疲劳、体弱)或直立性低血压风险的患者慎用。
7.7 代谢综合征 长期大量应用糖皮质激素可引起类肾上腺皮质功能亢进综合征,如水肿、低血钾、高血压、高血糖、皮肤变薄、向心性肥胖、多毛、痤疮、肌无力和肌萎缩等症状,一般无需特殊治疗,停药后可自行消退。但肌无力恢复缓慢且不完全。低盐、低糖、高蛋白饮食等措施可减轻上述症状。
总之,在预防和治疗呕吐的同时,还应注意止吐药物不良反应的预处理。虽然化疗引起的恶心和呕吐可明显影响患者的生活质量,并导致预后不良,但过度采取预防性止吐措施,特别是对轻微和低致吐风险的预防,可能使患者暴露于止吐药物的潜在不良反应并增加经济负担。加强治疗前宣教和治疗过程中的观察,与患者和家属充分沟通,特别是在出现不良反应后给予患者及时的心理疏导和对症处理是管理止吐药物不良反应的重要环节。止吐药物不良反应多数轻微且可控,如症状严重,除加强对症处理外,下一周期化疗时需对预防性止吐药物进行调整。
8 护理
8.1 用药护理 护士应了解抗肿瘤药物治疗所致不同类型恶心、呕吐的治疗原则、常用药物药理特性和给药方法,按时准确给药,有效预防和控制症状。止吐治疗后,及时进行疗效评价以调整治疗方案。
8.2 饮食和运动指导 根据患者的需求和病情需要调整饮食结构,进食以少量多餐、饮水以少量多次为宜。禁食刺激性食物和难以消化的食物。应以高热量、高蛋白、低脂、富含维生素、易消化的流质或半流质饮食为主。
结合患者体能评分、疾病状况和运动依从性等综合评估,鼓励患者化疗期间进行适度的有氧运动(慢跑、散步、快走等),有助于增加食欲,缓解恶心呕吐等不适症状。运动原则是循序渐进、量力而行。
8.3 环境准备 消除房间内的异味,如植物特殊气味、香水味等刺激性气味,以防刺激患者出现恶心、呕吐。保持房间内采光和通风良好,与病友保持良好的关系,调整与家属、朋友轻松进餐的气氛。
8.4 心理护理 及时掌握患者和家属的心理状态,做好患者的心理疏导,鼓励家属为患者提供精神心理支持,帮助患者正确认识和对待疾病,增强信心。可以通过音乐疗法、肌肉放松等行为训练缓解化疗期间恶心、呕吐。
8.5 健康教育和居家随访
8.5.1 健康教育 大部分化疗患者和家属对CINV认识不足,故健康教育尤其重要。病房除了建立抗肿瘤药物所致恶心呕吐相关规范化管理流程外,可通过一对一或集体面对面指导、宣教栏、宣教视频、宣教手册、宣教处方等多种形式向患者和家属做好教育指导。
8.5.2 建立居家随访制度 采用电话随访或建立微信群随访,随访时间从化疗开始至每疗程化疗结束后第5天。随访内容包括出院患者恶心、呕吐发生的时间、次数、呕吐物的量和内容物。了解患者因恶心、呕吐产生的心理影响,止吐治疗等情况,必要时指导患者返院或到当地医院治疗。
综上所述,恶心呕吐的处理原则应以预防为主,因为一旦发生较难控制,且易出现预期性恶心呕吐。恶心、呕吐的处理需要临床医生、护理人员、家属的共同努力,加强宣教和心理疏导,及时恰当地处理抗恶心、呕吐药物的不良反应,方能达到“无呕”的治疗目标。
共识组长
姜文奇 中山大学肿瘤防治中心
巴 一 天津医科大学肿瘤医院
冯继锋 江苏省肿瘤医院
共识执笔人
史艳侠 中山大学肿瘤防治中心
张 俊 上海交通大学医学院附属瑞金医院
沈 波 江苏省肿瘤医院
邢镨元 国家癌症中心,中国医学科学院肿瘤医院
共识专家组成员(按姓氏笔画排序)
王佳蕾 复旦大学附属肿瘤医院
仇晓霞 上海交通大学医学院附属仁济医院
巴 一 天津医科大学肿瘤医院
邓艳红 中山大学第六附属医院
石远凯 国家癌症中心,中国医学科学院肿瘤医院
史艳侠 中山大学肿瘤防治中心
冯继锋 江苏省肿瘤医院
邢镨元 国家癌症中心,中国医学科学院肿瘤医院
江泽飞 解放军总医院第五医学中心
孙 鹏 中山大学肿瘤防治中心
李志铭 中山大学肿瘤防治中心
杨顺娥 新疆医科大学新疆肿瘤医院
杨润祥 云南省肿瘤医院
邹本燕 中山大学肿瘤防治中心
沈 波 江苏省肿瘤医院
张 俊 上海交通大学医学院附属瑞金医院
张小田 北京大学肿瘤医院
张清媛 哈尔滨医科大学附属肿瘤医院
张群岭 复旦大学附属肿瘤医院
陈公琰 哈尔滨医科大学附属肿瘤医院
胡夕春 复旦大学附属肿瘤医院
侯 梅 四川大学华西医院
姜文奇 中山大学肿瘤防治中心
洪若熙 中山大学肿瘤防治中心
夏 青 上海交通大学医学院附属仁济医院
夏 莉 吉林省人民医院
郭桂芳 中山大学肿瘤防治中心
黄 欣 中山大学肿瘤防治中心
常建华 复旦大学附属肿瘤医院
程 颖 吉林省肿瘤医院
靳英辉 武汉大学循证与转化医学中心
蓝春燕 中山大学肿瘤防治中心
蔡修宇 中山大学肿瘤防治中心
共识秘书组
洪若熙 中山大学肿瘤防治中心
孙 鹏 中山大学肿瘤防治中心
张群岭 复旦大学附属肿瘤医院
夏 青 上海交通大学医学院附属仁济医院
仇晓霞 上海交通大学医学院附属仁济医院
参考文献:略
文章来源:《中国医学前沿杂志(电子版)》2019 年第11 卷第11 期
www.ahyllaw.com、安徽医疗纠纷律师、合肥医疗纠纷律师、安徽医疗事故律师、合肥医疗事故律师、安徽医疗律师、合肥医疗律师、医疗事故律师、医疗纠纷律师、陈俊福律师


